化学という学問のおもしろさは化学物質の電子状態を解明し,その電子状態の特性を理解した上で,それらを基礎として新奇な電子状態をもつ物質をデザイン・創出し,有益な物質して利用することであると考えている。化学の力を利用して新奇な電子状態を創り出すことは,触媒作用や吸着・分離現象への展開などにも関係し,大変興味深い,重要な研究であると認識している1)。無機物質の電子状態を操る魅力的な方法として,①構成原子中の電子の足し算を利用する方法2),②合金形成による方法3,4),③固体の表面や空間を利用した方法,④物質を微小化する(固体表面への物質の担持による)方法,⑤物質の欠陥(特に,表面欠陥)を利用する方法などがある5)。我々は,それらの中で,三番目の方法,特に種々の吸着・触媒現象に利用されているアルミノケイ酸塩であるゼオライトに注目した研究を行っている。ゼオライトは,現在をさかのぼること250年以上の1750年頃,天然ゼオライトが見いだされている。しかし,ゼオライトに関する画期的な進展は1948年,R. M. Barrerによる水熱合成法による人工ゼオライトの合成である。それ以来,230を超えるタイプのゼオライトが合成され,同時に応用へと展開され,化学工業分野での応用(物質合成のための触媒,イオン・気体分離材や吸着材等)を中心として,社会生活において必要不可欠な物質となっている。そして,構造・交換イオン・Al量などがそれぞれの過程で重要な役割を演じていることはよく知られており,既にわかりきった物質のように思われている節があるかもしれない。しかし,基礎化学的視点からすると,各過程でのゼオライトの役割の詳細はほとんどわかっていないと考える。それらの点が明らかになれば,ゼオライトの有用性は更に広範な分野に及ぶものと期待される。我々は,“ゼオライト空間が交換イオンに対して創り出す新奇な電子状態やその物質創製場としての利用”という観点から研究を進めてきた。このようにして創出された新奇な電子状態が,吸着現象や触媒作用における活性中心として機能していると考えている。更に,ゼオライト骨格によって創り出される空間を新奇物質の創製場として利用できるのである。ここでは,我々がこれまでの研究過程で見いだした現象を紹介しながら,それらの現象の起源となる交換金属イオンの状態やゼオライト場の役割および今後の研究展開などについても言及したい。
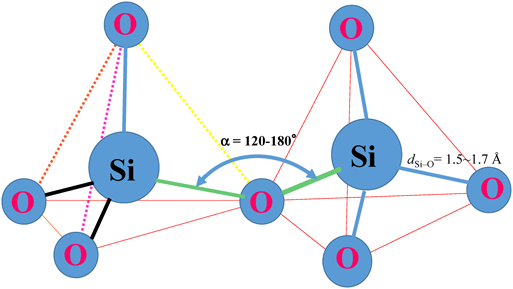
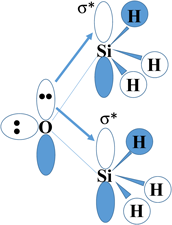
(a)ゼオライトはサイズの異なる細孔を含むアルミノシリケートからなる結晶性の物質である。一般に,SiO2の組成から構成される物資中のSi–O–Siの結合角には柔軟性があり,これは炭素からなるエーテル類(CnH2n+1–O–CnH2n+1)におけるそれとは性質が大きく異なる(CH3–O–CH3のCOCの角度は∠COC=120°付近である)。たとえば,H3Si–O–SiH3ではその角度は148°であり,Ph3Si–O–SiPh3では180°となる。このように,Si–O–Siの角度には多様性が有り,無機物質であるα-SiO2ではSi–O–Si角は144°であるが,トルトベイト石(Sc2Si2O7)では180°のものも知られている(Fig. 1)6–10)。これらの多様性は,当然,結晶性のゼオライトにおいても発現し,ゼオライトの細孔を形成する員環数や種々のゼオライトを形成するパーツにより,その物質特有の電子状態を創り出す要因の一つであると考えている。ゼオライトの場合を考えるとチャネルを形成する大きさ,即ち,曲率の効果といえるかもしれない。これらのSiO2を主な構成組成とする物質におけるSi–O–Siの角度への結合状態の効果を一般論として述べる。単純化したモデル(Fig. 2)で描いた系の電子状態の特徴は二つの(–SiH3)グループを橋かけしている酸素原子の塩基性度が,対応する炭素系,(CH3)2–O,の場合などに比べて,極めて低いことである。その理由は,Si系ではO上の不対電子が(–SiH3)上のσ*軌道に電子供与していることによると考えることができる11,12)。このような電子供与がC系では観測されない理由は,C–H間の結合がSi–H間のそれより強く,σ*反結合性軌道のエネルギー準位が高くなり,そのため電子供与が起こりにくいと考えることができる。この相互作用の存在のため,酸素原子と両端の(–SiH3)基との(p–σ*)軌道間において電子供与(p→σ*)が生じ,Si–O–Siの結合角はsp2混成の場合の120°付近からより広がるという結果になる。前述したように,酸化物中のSi–O–Siの結合角は140~160°付近の値が多く,化合物の中には180°の値をとる物質まで知られている。このような結合の特徴がゼオライト骨格の曲率に反映されることになると解釈できる。
(b)ゼオライト骨格にAlを導入することによって負電荷を生じさせる源となるAl元素の位置はゼオライトの特性創出の重要な役割を担う。Al原子導入により,生じた負電荷の電荷補償はプロトンや交換金属陽イオン等によってなされる。これらのイオンは種々の触媒反応や吸着サイトとして働くブレンステッド酸点(酸強度の異なる活性点となる)あるいは特異な電子状態を賦与された金属イオンとして機能する。この骨格に位置するAl原子の導入量(Si/Al比)や導入されたAlが占める位置や複数導入されたAl原子間の相互位置関係(分布)は種々の現象に於いて重要な役割を担う13–16)。そして,Alの分布はランダムではなくSi/Al比や合成条件に依存することが報告されている。しかし,Al原子の位置やその分布および導入されたAlの相互位置関係の詳細を正確に決定することは現状では困難である。近年では,X線回折測定の場合には,交換イオンとして重元素イオンを用い,その位置から間接的にAl位置や分布に関する情報が得られている17–23)。また,NMR法と計算化学的手法を併せて情報を得る方法などが提案されている24–30)。更に,最近,XAFS法も用いた研究の報告31–33)やWeckhuysenのグループが興味深い方法を報告している34)。
(c)大きさのそろった細孔:ゼオライトは規則的な細孔を有するという利点を生かし,酸・塩基サイトとして機能する金属イオン(シングルサイト,複合イオンサイト),金属ナノクラスターや金属酸化物の担体としても利用されている。特に,そのようにして形成された種の酸・塩基特性のコントロール,特異な電子状態,サイズのそろったチャネルが創り出す構造に起因した触媒活性能,生成物の選択性や形成種の安定性などが注目されている。
これらの特徴を反映したゼオライト系の特異な現象について,我々が見いだした系を中心に以下に簡単に紹介する。なお,この解説ではZnMFI系を中心に我々の研究内容の一部を簡単に紹介する。その他の例については別の解説などを参照頂きたい35–37)。
3. 亜鉛イオン交換MFI型ゼオライト(ZnMFI: Si/Al=11.9, イオン交換率ca. 95%)38–44)
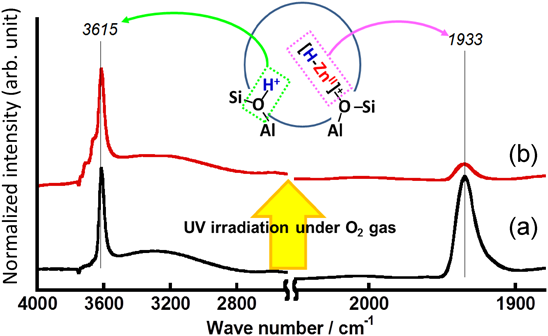
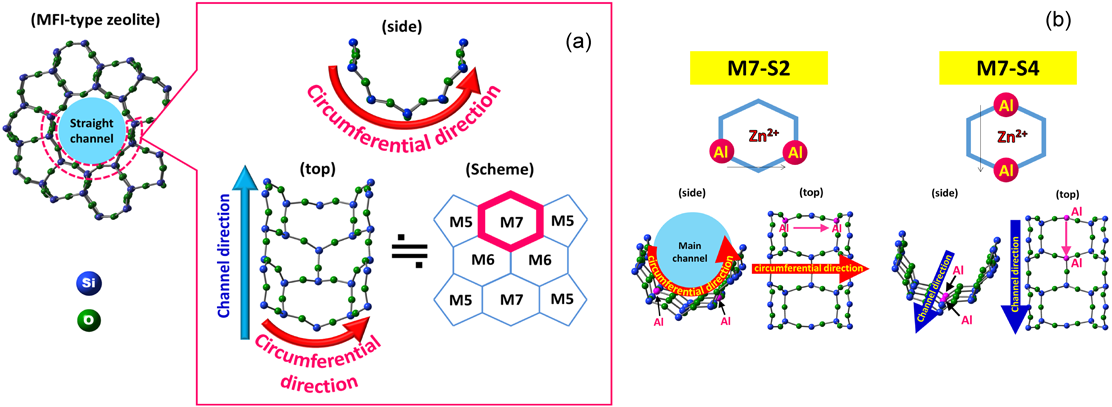
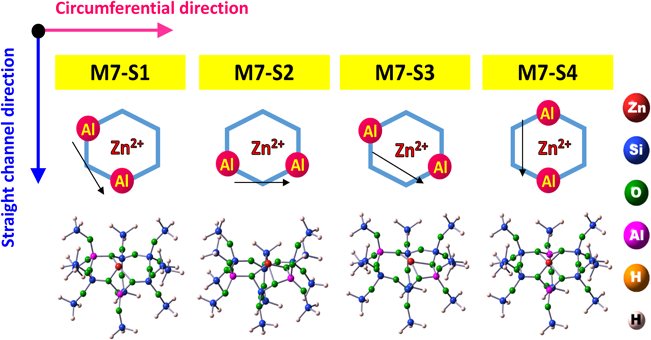
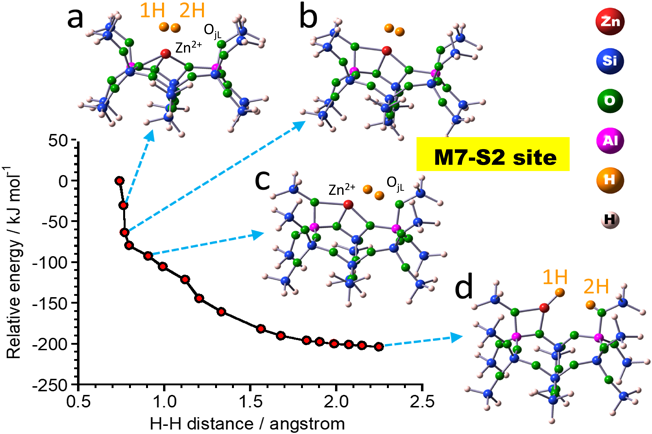
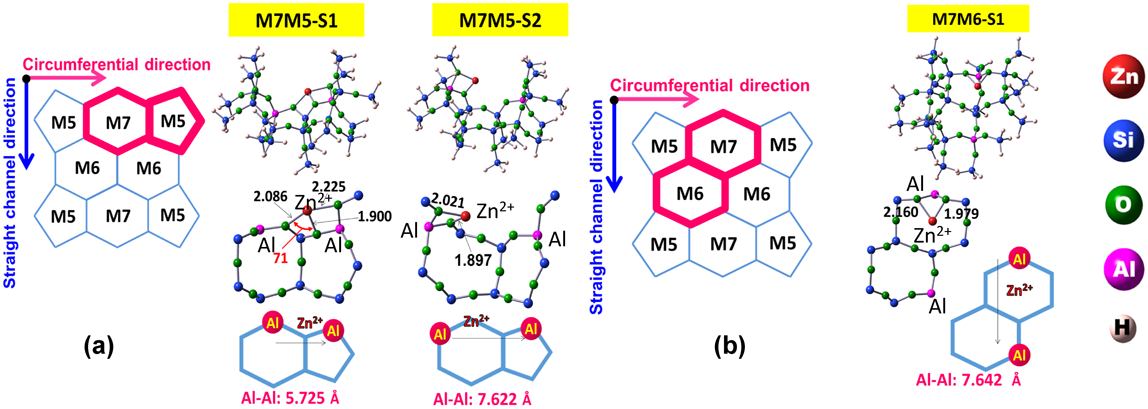
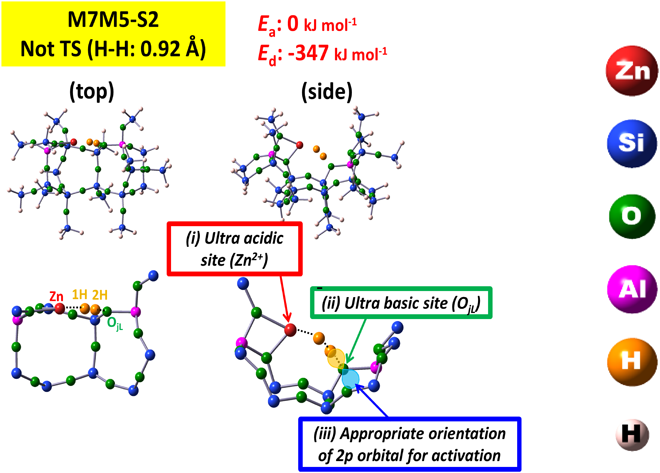
室温付近でさえ,交換Zn2+とH2分子との間に強い相互作用が生じ,結果として,H2の不均一結合開裂が生じ,–ZnHと–OH種が形成される。即ち, ZA–O–Zn2+–O–ZB+H2→ZA–O–ZnH++H+–O–ZBなる反応が生じる。この反応が生じていることは赤外線吸収スペクトルのデータから示唆される(Fig. 3a)。即ち,3615 cm−1に形成した–OH種によるバンド,1933 cm−1に形成した–ZnH種に帰属できるバンドが出現する。また,この試料上では,室温付近で,メタンの不均一結合開裂反応も進行することも明らかになった。これらの系について,活性点として機能するZn2+の状態を解明するために,H2不均一結合開裂反応をDFT計算によって再現を試みた。その過程では,ZnMFI系のH2の解離プロセスを提案する上で,Al配列が重要な役割を演じていると考え,異なるAl配置を有するいくつかのサイトのモデルを用いて,H2解離反応の過程に対して計算を行い,反応性の難易を調べた。まず,四種類の特異なAl–Alペアーサイト(MFIのストレートチャネル壁に存在するM7サイト内に二つのAl原子が特定の位置に占有されることによって創り出されるM7-S1~M7-S4サイト:Figs. 4,5)のモデルをつくった。それぞれのモデルでは,チャネル内でのAl–Alペアーサイトの配向が異なっている。図中の矢印でチャネル内の円周方向であるかチャネルの細孔に沿った方向であるのかを“ベクトル(図中に矢印)”で表示してある。Al–Alペアーサイトが細孔の円周方向に配向しているM7–S2サイトのZn2+上では水素分子が活性化を要しない過程で解離されることがわかった。また,その際の安定化エネルギーは204 kJ/molという値が得られた(Fig. 6)。これらの結果は室温で水素分子が開裂されるという実験事実と矛盾しない。他のサイトも含めて,エネルギープロファイルを求めた。その結果,M7–S2モデルについては,他のAl配列をもつモデルとは異なり,活性化エネルギーなしに反応が進行することがわかった。また,このM7-S2サイト上ではメタンの活性化現象についても,同様にうまく説明できる事もわかった。これらの事実は,提案したモデルの妥当性をより強固に肯定できる事実であると我々は主張している。更に,M7サイトに隣接するM5(Fig. 7a)員環サイトまたはM6(Fig. 7b)員環サイトにまたがってAl原子が配列するモデルでも検討した。これらの系の水素分子解離過程のエネルギープロファイルも算出した。それらの結果,M7M5–S1およびM7M5–S2サイト(Al–Al配列が細孔の円周上に位置する:ベクトル方向,矢印の方向,に注目)上では活性化過程なしで,水素分子の開裂が生じることがわかった。一方,細孔のチャネル方向にAl–Alが配列したM7M6–S1サイト(ベクトル方向に注目:Fig. 7b)上では活性化過程が存在し,水素分子の開裂には不利である事が明らかになった。これらの三種類のサイトの中で最も可能性の高いM7M5–S2サイト上での水素との相互作用の様子をFig. 8に示した。M7M5–S2サイト上での解離過程の安定化エネルギーが最も大きい(Ed=−347 kJ/mol: Fig. 8)ことが示された。その際,亜鉛イオンと骨格酸素とがそれぞれ酸点,塩基点として働き,水素分子の不均一結合開裂反応を有利に進める過程を構築することが明らかになった。我々はこれらの活性点をUltra acidic site(Zn2+)およびUltra basic site(Ojl)と提案している43)。また,観測された水素の活性化過程では骨格酸素のp軌道の方向が,相互作用の際,水素分子と直線状に相互作用することも重要な因子である(Fig. 8参照)。水素活性化と同一のモデルを用いることによって,メタンの活性化現象もうまく説明できる事も明らかになった。
ZnMFI系について,更に,Znイオン交換試料の調製法として,金属亜鉛を用い,それを真空下で熱処理により行った系では,二量体からなる[Zn–Zn]2+種の存在も確認できた。これらの亜鉛イオン交換試料の特徴を考慮すると,骨格中には比較的近接した位置にAl原子が存在することがこれらの現象で重要な因子であることが示唆される。この系の総ての現象は上述したAl配列をしたモデルを用いることによって,計算化学的手法で説明可能である。
これらの結果は,水素やメタンの活性化反応における交換カチオン周りの構造やその反応点としての役割はゼオライト中のAl原子の量やその位置(配向)に依存することは明らかであり,以上の様なモデル反応に計算化学的手法を適用すれば,Al原子の配置に関する知見が得られるものと期待できる。
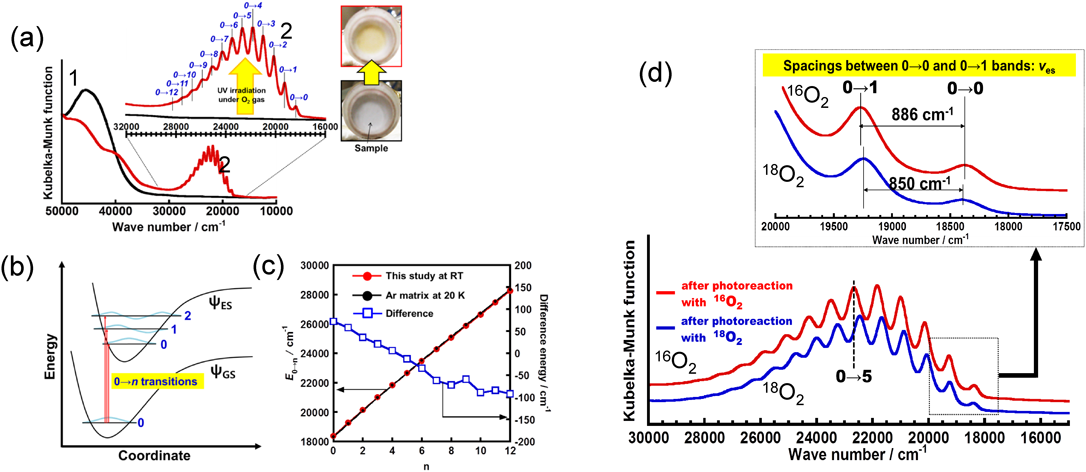
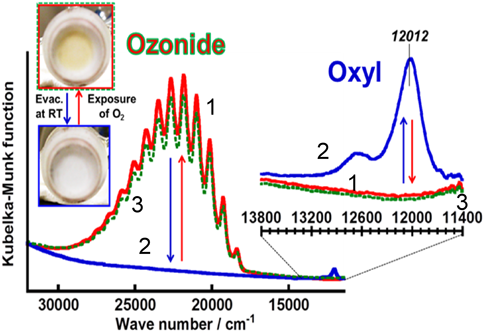
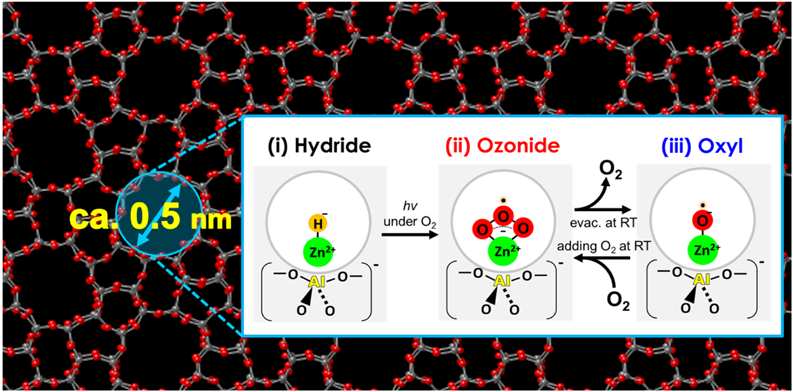
さて,上述した,室温で水素の不均一結合開裂反応により生じたZA–O–ZnH+種について,室温,酸素ガス存在下で紫外光照射すると1933 cm−1(νZn-H振動)のバンド強度は著しく減少し(Fig. 3b),同時に試料の色は白から黄色に変化する(Fig. 9a参照)。この過程のUV-Vis拡散反射スペクトルは,酸素ガス存在下紫外光照射により30000–16000 cm−1領域に極めて特徴的な微細構造を示すスペクトルを与える(Fig. 9a: spectrum 2)。この微細構造スペクトルは振動電子遷移(振電遷移)に由来するものと解釈できる。しかし,このような振電遷移が室温で観測できるという事実は極めて珍しいことである。この振電遷移の過程はFig. 9bに示した遷移モデルで表すことができる。この振電遷移部分に関して,更に情報を得るために,同位体酸素,18O2,を用いて実験を行った。測定したスペクトルをFig. 9dに示す。とくに,0–0遷移および0–1遷移(遷移のモデルはFig. 9b参照)部分の拡大図も示した。スペクトルの同位体シフトが観測されるという事実から,この振動遷移は吸着酸素種に関係した遷移に帰属できることは明らかである。また,この領域の吸収バンドの構造はArマトリックス(20 K)で測定された亜鉛オゾナイド種のそれと極めてよく一致する(Fig. 9c)45)。また,この吸収バンドは真空排気により消失することもわかった(Fig. 10)。この試料に室温で酸素を再度導入すると振電遷移由来のスペクトルは再生する。一方,Fig. 10に示した拡大図に示した12000 cm−1領域に注目すると,酸素導入後バンドはほとんど観測されない(spectra 1 and 3)。そして,再排気すると,強度の弱いバンドが観測されることがわかる(spectrum 2)。即ち,このバンドは排気することによって出現し,再度O2を導入することによって消失することがわかる。これらの過程で試料の色は変化する。酸素の排気で,試料の色は黄色から白色に変化する(Fig. 10参照)。この排気過程で生じた種は亜鉛オキシル種であると考えた。12000 cm−1付近に観測される数本のバンドは亜鉛オキシル種の振動遷移であると考え,DFT計算により,その解釈の妥当性を検討した。その結果,同位体酸素を用いた場合,16O2および18O2,それぞれの振動バンド解析は606, 575 cm−1付近の振動構造が得られたことから,それらはZn2+–O(オキシル)種の振動遷移に帰属できることが証明された。これらのことから,本系では酸素導入/紫外光照射処理により[ZnII–(η2)O3·]+種(オゾナイド種)が生じ,その種は室温で真空排気することによって,分解し,[ZnII–O·]+種(新奇なオキシル種)に変化するという,極めて奇妙でめずらしい反応が起こることがわかった。この一連の反応は,以下に示すように,室温下で酸素存在の有無で可逆的に進行することも明らかになった。通常,不安定で室温では検出されていないオキシル種がゼオライト中で形成され,しかも室温でさえ安定に存在するという特異な例である。
[ZnII–O·]+(S=1/2)+O2(S=1) ⇄ [ZnII−(η2)O3·]+(S=1/2)
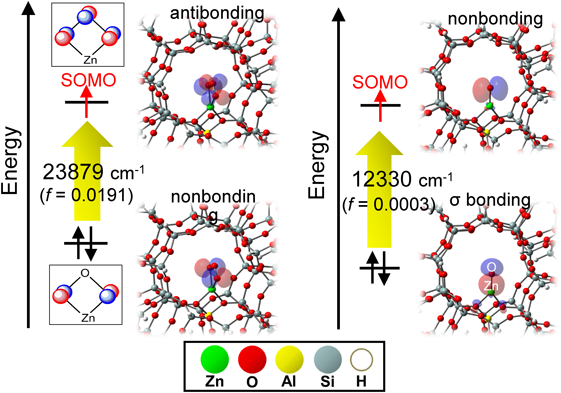
これらの過程で観測される特徴的な可視光−近赤外線領域のバンド(23000 cm−1付近および12000 cm−1付近)の帰属はDFT計算の結果から,[ZnII–(η2)O3·]+(オゾナイド種)と[ZnII–O·]+(オキシル種)による遷移に帰属できる(遷移の帰属の詳細はFig. 11参照)。実際観測されるスペクトルでは,Fig. 10に示したように,可視部の領域にオゾナイド種と近赤外線部の領域にオキシル種による吸収バンドが観測され,それぞれの種による振動遷移構造が各吸収バンドに重なって観測されているということになる。以上の結果をまとめ,提案した種とその変化過程をFig. 12にスキームとして示した。以上,極めて,特異な興味深い結果である。まさに,ゼオライト場を利用した新奇電子状態の創出であると考える。このオキシル種はラジカル状態で有り,メタンなどの不活性気体の活性化も可能であると考えている。
4. NiMFI中に形成されたNi6クラスターの特徴
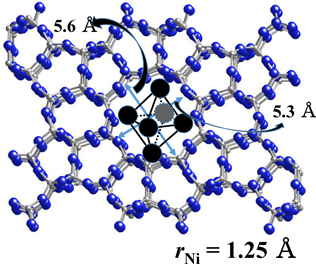
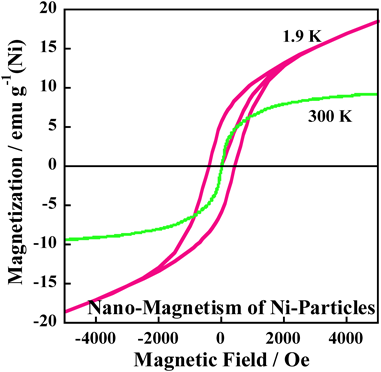
近年クラスター種や微粒子の物性や触媒作用の特異性に関する研究が盛んに行われている。これらのクラスター種は安定ではなく,容易に集合化し,大きなクラスターとなり,特異な物性や触媒作用は簡単に失われてしまうことが知られている。Iglesiaの研究チームなどは2010年以降,ゼオライト空間を利用し,そのサブナノサイズの空間内にクラスター種を調製し,その触媒特性の研究を行っている46,47)。さらに,微粒子,表面上に形成された薄膜状の物質や固体表面に担持した試料の興味深い磁気特異性発現に関する研究例もある48–51)。ここでは,Sub-nanoサイズの細孔を利用した,磁気特性に関する我々が行った研究例を簡単に紹介する。上述したように,表面に形成されたクラスターや薄膜はバルクの磁気特性と異なる特性を示す場合がある。我々は,ゼオライトサブナノ空間中に金属クラスター種を調製したときに,どのような特異な磁気特性が発現するのかという点に興味をもった。そこで,ゼオライトを利用したクラスター種の形成をめざした。バルクニッケルは強磁性の性質を有することがよく知られている。このNiを微粒子化したときに,どのような磁気特性を示すかという点に注目した。NiII-MFI試料を真空加熱することによって脱水し,NiII–O–NiII種に変化させ,その後,CO処理によりNi2+をNi+種とし,さらに,673 Kで再排気すると不均化反応が起こり,Niクラスター種が細孔中に形成されることを見いだした。EXAFSの解析などにより(Ni6)0クラスターが形成されることがわかった(Fig. 13)。また,この種は酸化,その後CO処理,再排気を経ると(Ni6)0種が再生できることが明らかになった。このようにして形成された(Ni6)0種は超常磁性の性質を示すことがわかった。即ち,このクラスター種は室温ではヒステリシスを与えないけれども,低温ではヒステリシスを示した。また,低温で測定した磁気特性(飽和磁化率,残留磁化,抗磁力など)の値がバルクのそれらより大きいという,興味深い特徴を有することがわかった(Fig. 14)。この系の触媒作用についても興味がもたれる。
種々のイオン交換ゼオライトについて,活性点の状態とAl配列との相関を明らかにすることは,既存のゼオライト触媒の性能を高めるために,また新触媒の設計指針を得る上で不可欠な研究であると考える。Al配置(異なるAl配列),骨格と交換イオンの相互作用,ゼオライトのタイプ,それらの試料中のSi–O–Siの角度,酸性度,交換イオンのダイナミクスなどに関する知見は,ゼオライトの特性を最大限に引き出すための基本情報であり,近年,これらの分野での研究が精力的になされている14–16,52–57)。また,最近,ゼオライトの薄膜を調製し,その状態を高真空下で構造・電子状態を分子レベルで研究する方法も行われている58–60)。これらの研究が発展し,ゼオライトの化学研究がより進展することを期待する。
謝辞Acknowledgments
本稿で述べた研究成果はさきがけ研究員の織田晃博士(岡山大学大学院自然科学研究科客員研究員)が精力的に行った研究成果の一部をまとめたものである。また,本研究は大久保貴広准教授(岡山大学),小林久芳教授(現:京都工芸繊維大学名誉教授)および湯村尚史准教授(京都工芸繊維大学)との共同研究として行うことによって成就した。本研究は科研費(2155021, 16H04118)の助成を受け,行うことができた。
引用文献References
1) N. Fischer, H. G. Manyar, A. Roldan, Chem. Commun., 52, 8335(2016).
2) Z. Luo, A. W. Castleman, Acc. Chem. Res., 47, 2931(2014).
3) H. Kobayashi, K. Kusada, H. Kitagawa, Acc. Chem. Res., 48, 1551(2015).
4) S. Furukawa, T. Komatsu, ACS Catal., 7, 735(2017).
5) C.-Y. Wu, W. J. Wolf, Y. Levartovsky, H. A. Bechtel, M. C. Martin, F. D. Toste, E. Gross, Nature, 541, 511(2017).
6) G. V. Gibbs, M. M. Hamil, S. J. Louisnathan, L. S. Bartell, H. Yow, Amer. Mineral., 57, 1578(1972).
7) D. M. Hatch, S. Ghose, Phys. Chem. Minerals, 17, 554(1991).
8) R. J. Gillespie, S. A. Johnson, Inorg. Chem., 36, 3031(1997).
9) F. Weinhold, R. West, Organometallics, 30, 5815(2011).
10) R. J. Gillespie, S. A. Johns Sanchez-Smith, P. Rez, M. O’Keeffe, M. M. Treacy, Chem. Mater., 26, 1523(2014).
11) 例えば,NH3分子の分子軌道図を参照のこと:友田修司 著 基礎量子化学―軌道概念で化学を考える― 東京大学出版会(2007).
12) M. Weller, T. Overton, J. Rourke, F. Armstrong, Inorganic Chemistry, 6th Ed. 2014, Oxford, UK.
13) J. Dědeček, Z. Sobalík, B. Wichterlová, Catal. Rev.: Sci. Eng., 54, 135(2012).
14) C. Paolucci, J. R. Di Iorio, F. H. Ribeiro, R. Gounder, Adv. Catal., 59, 1(2016).
15) M. L. Bols, S. D. Hallaert, B. E. R. Snyder, J. Devos, D. Plessers, H. M. Rhoda, M. Dusselier, R. A. Schoonheydt, K. Pierloot, E. I. Solomon, B. F. Sels, J. Am. Chem. Soc., 140, in press(2018): DOI: 10.1021/jacs.8b05877.
16) E. Borfecchia, P. Beato, S. Svelle, U. Olsbye, C. Lamberti, S. Bordiga, Chem Soc. Rev., in press(2018): DOI: 10.1039/c8cs00373d.
17) D. H.Olson, J. Phys. Chem. B, 104, 4844(2000).
18) B. F. Mentzen, G. Bergeret, H. Emerich, H.-P. Weber, J. Phys. Chem. B, 110, 97(2006).
19) B. F. Mentzen, G. Bergeret, H. Emerich, H.-P. Weber, J. Phys. Chem. B, 110, 13741(2006).
20) B. F. Mentzen, G. U. Rakhmatkariev, G. Bergeret, H.-P. Weber, J. Phys. Chem. C, 111, 3820(2007).
21) B. F. Mentzen, G. Bergeret, J. Phys. Chem. C, 111, 12512(2007).
22) B. F. Mentzen, J. Phys. Chem. C, 111, 18932(2007).
23) N. H. Heo, C. W. Kim, H. J. Kwon, G. H. Kim, S. H. Kim, S. B. Hong, K. Seff, J. Phys. Chem. C, 113, 19937(2009).
24) J. R. Di Iorio and R. Gouder, Chem. Mater., 28, 2236(2016).
25) C. Paolucci, I. Khurana, A. A. Parekh, S. Li, A. J. Shih, H. Li, J. R. Di Iorio, J. D. Albarrachin-Caballero, A. Yezerets, J. T. Miller, W. N.Delgass, F. H. Ribeiro, W. F. Schneider, R. Gounder, Science, 357, 898(2017).
26) J. Dědeček, D, Kaucký, B. Wichterlová, O. Gonsiorová, Phys. Chem. Chem. Phys., 4, 5406(2002).
27) B. Lu, T. Kanai, Y. Oumi, T. Sano, J. Porous Mater., 14, 89(2007).
28) A. Janda, A. T. Bell, J. Am. Chem. Soc., 135, 19193(2013).
29) J. Dědeček, S. Sklenak, C. Li, B. Wichterlová, V. Gábová, J. Brus, M. Sierka, J. Sauer, J. Phys. Chem. C, 113, 1447(2009)
30) J. Dědeček, S. Sklenak, C. Li, F. Gao, J. Brus, Q. Zhu, T. Tatsumi, J. Phys. Chem. C, 113, 14454(2009).
31) R. W. Joyner, A. D. Smith, M. Stockenhuber, M. W. E. Van den Berg, Phys. Chem. Chem. Phys., 6, 5435(2004).
32) I. J. Drake, Y. Zhang, M. K. Gilles, C. N. T. Liu, P. Nachimuthu, R. C. C. Perera, H. Wakita, A. T. Bell, J. Phys. Chem. B, 110, 11665(2006).
33) A. Vjunov, J. L. Fulton, T. Huthwelker, S. Pin, D. Mei†, G. K. Schenter, N. Govind, D. M. Camaioni, J. Z. Hu, J. A. Lercher, J. Am. Chem. Soc., 136, 8296(2014).
34) J. E. Schmidt, L. Peng, J. D. Poplawsky, B. M. Weckhuysen, Angew. Chem. Int. Ed., 57, 10422(2018).
35) 織田晃,鳥越裕恵,黒田泰重,触媒,55, 352(2013).
36) 織田晃,鳥越裕恵,黒田泰重,ゼオライト,31, 88(2014).
37) 黒田泰重,Adsorption News, 32, 3(2018).
38) A. Oda, H. Torigoe, A. Itadani, T. Ohkubo, T. Yumura, H. Kobayashi, Y. Kuroda, Angew. Chem. Int. Ed., 51, 7719(2012).
39) A. Oda, H. Torigoe, A. Itadani, T. Ohkubo, T. Yumura, H. Kobayashi, Y. Kuroda, J. Am. Chem. Soc., 135, 18481(2013).
40) A. Oda, H. Torigoe, A. Itadani, T. Ohkubo, T. Yumura, H. Kobayashi, Y. Kuroda, J. Phys. Chem. C, 117, 19525(2013).
41) A. Oda, H. Torigoe, A. Itadani, T. Ohkubo, T. Yumura, H. Kobayashi, Y. Kuroda, J. Phys. Chem. C, 118, 15234(2014).
42) A. Oda, T. Ohkubo, T. Yumura, H. Kobayashi, Y. Kuroda, Dalton Trans., 44, 10038,(2015).
43) A. Oda, T. Ohkubo, T. Yumura, H. Kobayashi, Y. Kuroda, Phys. Chem. Chem. Phys., 19, 25105(2017).
44) A. Oda, T. Ohkubo, T. Yumura, H. Kobayashi, Y. Kuroda, Angew. Chem. Int. Ed., 56, 9715(2017).
45) E. S. Prochaska and L. Andrews, J. Chem. Phys., 72, 6782(1980).
46) M. Choi, Z. Wu, E. Iglesia, J. Am. Chem. Soc., 132, 9129(2010).
47) N. Wang, Q. Sun, R. Bai, X. Li, G. Guo, J. Yu, J. Am. Chem. Soc., 138, 7484(2016).
48) H. Hori, T. Teranishi, Y. Nakae, Y. Seino, M., Miyake, S. Yamada, Phys. Letts. A, 263, 406(1999).
49) T. Shinohara, T. Sato, T. Taniyama, Phys. Rev. Letts., 91, 197201(2003).
50) M. Zheng, L. Menon, H. Zeng, Y. Liu, S., Bandyopadhyay, R. D. Kirby, D. J. Sellmyer, Phys. Rev. B, 62, 12282(2000).
51) F. C. Fonseca, G. F. Goya, R. F.; Jardim, R. Muccillo, N. L. V. Carreno, E. Longo, E. R. Leite, Phys. Rev. B, 66, 104406(2002).
52) B. E. R. Snyder, M. L. Bols, R. A. Schoonheydt, B. F. Sels, E. I. Solomon, Chem. Rev., 118, 2718(2018).
53) K. T. Dinh, M. M. Sulliva, P. Serna, R. J. Meyer, M. Dincǎ, Y. Román-Leshkov, ACS Catal., 8, 8306(2018).
54) J. Brus, L. Kobera, W. Schoefberger, M. Urbanová, P. Klein, P. Sazama, E. Tabor, S. Sklenak, A. Fishchuk, J. Dědeček, Angew. Chem. Int. Ed., 54, 541(2015).
55) F. Blanc, Angew. Chem. Int. Ed., 56, 11694(2017).
56) K. Muraoka, W. Chaikittisilp, Y. Yanaba, T. Yoshikawa, T. Ohkubo, Angew. Chem. Int. Ed., 57, 3742(2018).
57) M. Dusselier, M. E. Devis, Chem. Rev., 118, 5265(2018).
58) J. A. Boscoboinik, X. Yu, B. Yang, F. D. Fischer, R. Włodarczyk, M. Sierka, S. Shikhutdinov, J. Sauer, H.-J. Freund, Angew. Chem. Int. Ed., 51, 6005(2012).
59) R. Włodarczyk, J. Sauer, X. Yu, J. A. Boscoboinik, B. Yang, S. Shikhutdinov, H.-J. Freund, J. Am. Chem. Soc., 135, 19222(2013).
60) H. Tissot, L. Li, S. Shikhutdinov, H.-J. Freund, Phys. Chem. Chem. Phys., 18, 25027(2016).