日本では国内及び海外から調達された年間約9,000万トンの農林水産物が食品として活用されているが,その中の約1,900万トン(食品関連事業者から約800万トン,一般家庭から約1,100万トン)が食品廃棄物として排出されている。食品廃棄物には調理くずなどの食材として適さないものだけでなく,本来は食べられるにもかかわらず廃棄されているものが含まれている。この“食品ロス”は年間約500万~900万トンと推計されており,食用向け農林水産物の約5~10%,食品由来廃棄物の約30~50%を占めると推計されている。世界的な人口増加やアジア諸国の経済発展による食料需要の増大など,世界の食料需給の不安定要因が顕在化する中で,食品ロスの改善は日本のみならず世界的にも大きな課題となっている。
食物の貯蔵および物流技術が目覚ましく発達した現代では,北方の国々でも南国のフルーツが比較的容易に入手できる。一方,長期間にわたる食品輸送および貯蔵の観点からは如何に食品の成熟を抑制して鮮度を保持できるかが重要であり,この課題は食品ロスの問題を解決する上でも大きな命題となっている。植物ホルモンとして知られるエチレンはごく低濃度でも野菜や果物の成熟を促進するため,その除去方法が活発に検討されてきた1–3)。エチレンの特徴は非常に高い生理活性にあり,例えば多くの果物(アボガド,バナナ,メロン,マンゴーなど)の成熟促進に必要とされるエチレン濃度は0.1~1.0 µL L−1(ppm)という極めて低濃度である1)。エチレンは貯蔵中の食品自身から発生するため,食品の熟成を抑制するためには保存容器内におけるエチレンの完全分解または吸着除去技術の確立が求められてきた。代表的なエチレン除去方法は,吸着材を利用した吸着分離技術である。活性炭やゼオライトなどの吸着材は他の有機分子と同様にエチレンを吸着する能力を示すが,吸着容量には限界があるため密閉容器内におけるエチレンの定常的な除去方法として利用することは難しい2)。量論的な化学反応を利用したエチレン分解も報告されているが,この手法の欠点は有効な除去期間が投入する試薬量に依存してしまうことである。
一方,触媒法による酸化分解は定常的にエチレンを除去する技術として有用である。近年,固体触媒による低濃度エチレンの完全分解が検討されている。今中らは,白金粒子を担持した固体酸化物触媒(Pt/Ce0.64Zr0.16Bi0.20O1.90/γ-Al2O3)が1%エチレンガスを65°Cにて完全分解できることを報告した4)。アルミナ担持白金触媒(Pt/γ-Al2O3)は145°C以上でエチレンを二酸化炭素と水へ分解するが,アルミナ担体へ酸素吸蔵・放出能を有するCe0.64Zr0.16Bi0.20O1.90をドープすることによって分解温度を大幅に低下させることに成功した。また,Qiaoらはメソポーラス酸化コバルト担持金触媒(Au/mesoporous Co3O4)が0°Cにおいて低濃度エチレン(50 ppm)を効率よく酸化分解(転化率:76%)できることを見出した5,6)。さらに,ロッド状酸化コバルトを担体とすることにより担持した金ナノ触媒のエチレン分解活性は94%へと向上した7)。これらの固体触媒はいずれも有用なエチレンの酸化分解触媒であるが,食品貯蔵への応用という側面では低濃度エチレンを完全分解できる固体触媒の開発が期待されている。
我々はこれまでに,低濃度COの酸化反応に対してメソポーラスシリカ担持白金触媒が高い触媒活性を示すことを見出した。メソポーラスシリカ担持白金触媒の高い触媒活性は,白金粒子とシリカ細孔壁の界面に存在する水酸基がCOとO2を逐次的に活性化することに起因している8,9)。もしエチレン酸化分解がWacker型反応によって進行した場合,生成したアルデヒドはCOを経てCO2へと酸化されると考えられる。また,メソポーラスシリカ表面に存在するシラノールの特異的な反応性は,エチレンを含む他の炭化水素類の活性化への寄与も期待できる。そこで我々は,メソポーラスシリカ担持白金触媒を用いて低濃度エチレンの低温酸化分解を検討したところ,0°Cにおいて低濃度エチレン(50 ppm)を完全分解することを発見した10)。本稿では,メソポーラスシリカを担持とした金属触媒の合成と構造解析,低濃度エチレンの酸化分解反応に対する触媒活性について概説する。さらに赤外分光分析を用いて,白金ナノ粒子表面におけるエチレン分解の反応メカニズムを解析した結果についても紹介する。
2. メソポーラスシリカ担持金属触媒によるエチレン酸化反応
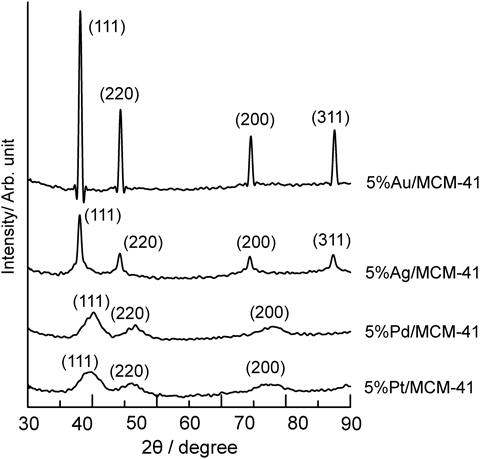
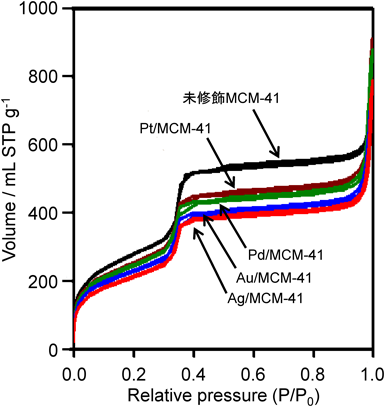
メソポーラスシリカであるMCM-41を担体とし,4種類の金属ナノ粒子(Au, Ag, Pd, Pt)を固定した担持金属触媒を調製した。MCM-41に対してそれぞれの水溶性塩化物塩を用いて5 wt%になるよう金属種を含浸担持し,その後の200°Cにおける水素還元処理によりシリカ表面にナノ粒子を生成させた8)。シリカ表面に析出した金属粒子の構造をXRDによって評価した(図1)。すべての試料で対応する金属種の面心立方格子(Face-centered cubic, FCC)構造に由来する回折パターンが観測された。表1には,これらの回折シグナルとシェラー(Scherrer)式によって算出した金属の平均粒子径を示す。PdおよびPtの平均粒子径はブロードな回折ピークを反映し,2.4 nmおよび3.7 nmと見積もられた。一方,AuおよびAgは比較的大きな平均粒子径を有しており,細孔サイズの小さなMCM-41の細孔内へは固定できないと考えられる。そこで,金属ナノ粒子による細孔閉塞の影響を確かめるため,窒素吸着測定によって試料の表面積および細孔径を評価した。図2および表1には,試料の吸着等温線と表面積・平均細孔径を示す。すべての試料が典型的なⅣ型の等温線11)を示しており,その表面積は770~920 m2 g−1,平均細孔径は2.8~2.9 nmであった。これらの物性値は既報のMCM-41と同等であり,金属粒子を担持後も基本的な細孔特性は保持されていた。XRDで見積もった金属粒子サイズと細孔径を考慮すると,Pt粒子のみが細孔内部に高分散担持されていると考えられる。Pd/MCM-41も細孔径以下の粒子はメソ孔内部に固定されているが,3 nmを上回るサイズの粒子は細孔を閉塞することなく外表面に固定されたと考えられる。一方,大部分の金属粒子が細孔サイズを大幅に上回ったAu/MCM-41およびAg/MCM-41では,大きな金属粒子が閉塞することなく外表面のみに固定された。Pt/MCM-41のPt粒子サイズは透過電子顕微鏡(Transmission electron microscopy, TEM)による観察からも算出した。図3に示したPt/MCM-41のTEM写真では,細孔内部に白金ナノ粒子が分散担持されている様子が直接確認された。TEM観察によって見積もったPt粒子サイズは2.9±0.7 nmとなり,XRD回折から求めた金属粒子径と一致した。
表1 メソポーラスシリカ担持金属触媒の物性値| 触媒 | SBET[a]/m2 g−1 | 細孔径[b] | 金属粒子径/nm |
| XRD[c] | TEM[d] |
| 5%Pt/MCM-41 | 913 | 2.9 | 2.4 | 2.9±0.7 |
| 5%Pd/MCM-41 | 889 | 2.8 | 3.7 | Not measured |
| 5%Ag/MCM-41 | 770 | 2.8 | 23 | Not measured |
| 5%Au/MCM-41 | 822 | 2.8 | 35 | Not measured |
| [a] BET表面積,[b] BJH式によって算出した平均メソ細孔径,[c] シェラー式を使ってXRD回折パターンから見積もった金属粒子径,[d] TEMによって見積もった金属粒子径 |
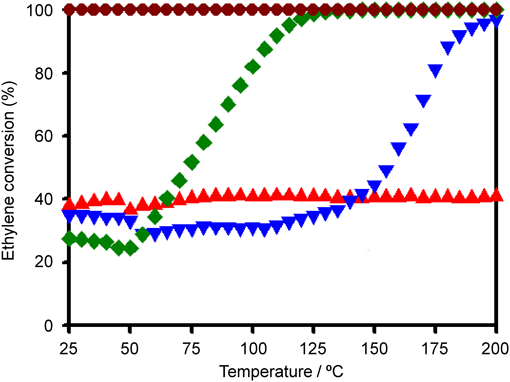
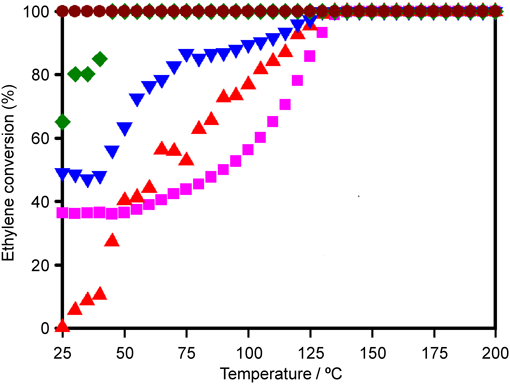
試料の触媒活性を,固定床流通反応装置を用いたエチレン酸化反応によって評価した。担持金属触媒(0.20 g)をステンレス製反応容器に充填し,空間速度1500 mL h−1 g−1 (C2H4 : 0.32 vol%, O2 : 20 vol%, N2 : 5 vol%, He : バランス)の条件にて触媒反応を実施した。図4には,25–200°Cにおける試料のエチレン転化率の変化を示す。Pt/MCM-41は全温度領域において転化率>99.9%を示しており,エチレン酸化反応に対して極めて高い触媒活性を示した。一方,他の担持金属触媒は25–50°Cの領域で転化率40%以下となり,50°C以上の反応温度に対する依存性は大きく異なった。Pd/MCM-41は50°C以上から徐々にエチレン転化率が上昇し,125°C以上で転化率>99.9%を示した。Ag/MCM-41は全温度領域で一定の転化率(約40%)を示したのに対し,Au/MCM-41のエチレン転化率は150°C付近から徐々に上昇し200°Cで95%以上となった。よって,メソポーラスシリカ担持白金触媒がエチレン酸化反応に対して特異的に高い触媒活性を示すことが明らかになった。
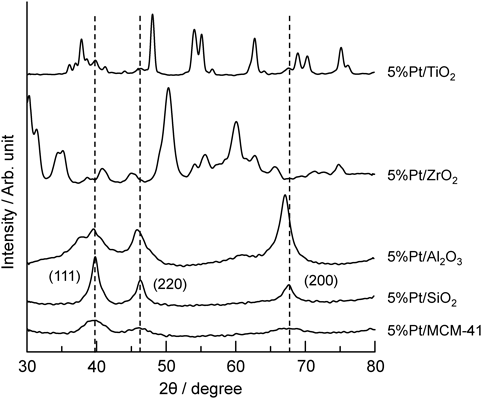
次に,様々な担体を用いて担持白金触媒を調製し,そのエチレン酸化活性を評価した。非規則多孔性のSiO2,TiO2,Al2O3,ZrO2に対してMCM-41と同様の含浸法により導入量が5 wt%になるように白金を担持した。図5には得られた試料のXRDパターンを示す。Pt/SiO2ではPt/MCM41と同様に白金粒子のFCC構造に帰属される回折ピークが見られたのに対し,他の試料ではPt粒子の回折ピークがそれぞれの担体酸化物の結晶構造の回折ピークと重複していた。そのため,酸化物表面に形成された白金粒子径サイズをXRD回折ピークから単純に見積もることはできない。よって,COパルス測定およびTEM観察によって形成された白金の粒子径を評価した。表2には, 試料のCOパルス測定から得られた金属分散度と平均粒子径をまとめた12,13)。大きな表面積を有するPt/MCM-41は,高い金属分散度(0.38)と小さなPt粒子径(3.0 nm)を示した。4種類の酸化物担体の表面積はMCM-41よりも大幅に小さいが,その分散度と粒子径は表面積には依存しない傾向となった。Pt/SiO2とPt/TiO2はMCM-41よりも小さな金属分散度を示しており,試料表面の白金粒子径も約5 nm程度となった。一方,Pt/Al2O3およびPt/ZrO2の表面積はMCM-41の1/6程度であるが,Pt/MCM-41を大きく上回る高い金属分散度を示しており,その白金粒子径は約2.5 nmと見積もられた。図6には試料のTEM写真を示す。すべての試料でバルク酸化物粒子の表面に白金粒子が形成されており,その粒子径はCOパルス測定で見積もられた値を支持する結果となった。なお,Pt/SiO2の白金粒子径はXRDの回折シグナルからシェラー式によって見積もった白金粒子径とも良い一致を示した(表2)。
表2 担持白金触媒の物性値
| 触媒 | SBET[a]/m2 g−1 | 金属分散度[b] | 金属粒子径/nm |
| CO吸着[c] | XRD[d] | TEM[e] |
| 5%Pt/MCM-41 | 913 | 0.38 | 3.0 | 2.4 | 2.9±0.7 |
| 5%Pt/SiO2 | 270 | 0.25 | 4.6 | 5.8 | 4.3±1.2 |
| 5%Pt/Al2O3 | 143 | 0.44 | 2.6 | — | 2.0±1.0 |
| 5%Pt/ZrO2 | 72 | 0.50 | 2.3 | — | 1.2±0.5 |
| 5%Pt/TiO2 | 52 | 0.20 | 5.7 | — | 2.8±1.1 |
| 1%Pt/MCM-41 | 820 | 0.51 | 2.2 | 1.7 | 2.0±0.6 |
| [a] BET表面積,[b] COバルス測定によって見積もった50°Cにおける金属分散度,[c] 金属粒子径 (ρcalcd)=1.13/D(D: CO/Ptから見積もった金属分散度),[d] シェラー式を使ってXRD回折パターンから見積もった金属粒子径,[e] TEMによって見積もった金属粒子径 |
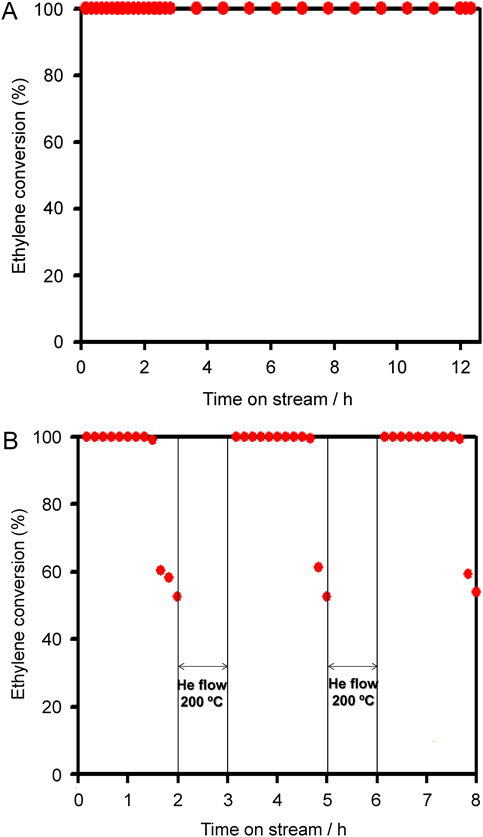
これらの試料の触媒活性を,固定床流通反応装置を用いたエチレン酸化反応によって評価した。図7には,試料の25–200°Cにおけるエチレン転化率の変化を示す。すでに示したように,Pt/MCM-41は全温度領域において転化率>99.9%を示した。3種類の担持白金触媒(Pt/Al2O3, Pt/TiO2, Pt/ZrO2)も125°C以上の温度域では転化率>99.9%を示すが,125°C以下では徐々にエチレン転化率が低下した。Pt/SiO2は他の触媒に比べて低温領域でも高いエチレン転化率を示し,25°Cにおけるエチレン転化率は他の担持触媒より高活性(転化率>60%)となった。しかし,25°Cにおいてエチレンの完全分解が可能だったのはPt/MCM-41のみだった。よって白金担持量を1 wt%としたPt/MCM-41を合成し,25°Cと0°Cにおける低濃度エチレンの分解活性を詳細に検討した。合成したPt(1 wt%)/MCM-41はMCM-41特有の細孔体特性(表面積:820 m2 g−1,細孔径:2.8 nm)と高い金属分散度(0.51)を有している14)。Pt(1 wt%)/MCM-41の白金粒子径は,COパルス測定,XRD測定,TEM観察から約2 nmと見積もられた。また,担持した白金粒子はPt(5 wt%)/MCM-41と同様に細孔内部に高分散担持されていた(図9(A))。図8には,25°Cおよび0°Cにおけるエチレン酸化反応の経時変化を示す。担持金属触媒(0.40 g)をステンレス製反応容器に充填し,空間速度1500 mL h−1 g−1(C2H4 : 50 ppm, O2 : 20 vol%, N2 : 5 vol%, He : バランス)の条件にてエチレン酸化反応を実施した。Pt(1 wt%)/MCM-41は25°Cにおいて12時間にわたりエチレン転化率>99.9%を保持した。50 ppmという低濃度エチレンに対してPt(1 wt%)/MCM-41は長時間にわたって安定した酸化除去活性を示しており,実用触媒としての高いポテンシャルを示した。そこで,次に反応温度を0°Cに設定してPt/MCM-41の触媒活性を評価した。Pt(1 wt%)/MCM-41は反応初期から1時間以上にわたって99.8%以上の高いエチレン転化率を示したが,その活性は徐々に低下した。この活性低下はエチレン酸化によって生成した水分子が白金粒子へ吸着したことに起因している。活性低下した触媒をヘリウム気流下にて200°Cで加熱すると,白金サイトを被毒している吸着水が除去されて初期活性が回復した。再生したPt/MCM-41は長時間にわたって高いエチレン転化率を示し,3回目の繰り返し反応においても活性低下は見られなかった。反応前後の試料の局所構造をTEMによって観察したところ(図9),細孔構造の規則性低下や白金ナノ粒子の凝集または粒子径の拡大なども確認されなかった。よって,Pt/MCM-41は0°Cにおける低濃度エチレン(50 ppm)の酸化分解に対して安定で高い触媒活性を示す固体触媒である。
4. Pt/MCM-41におけるエチレン酸化分解のメカニズム解析
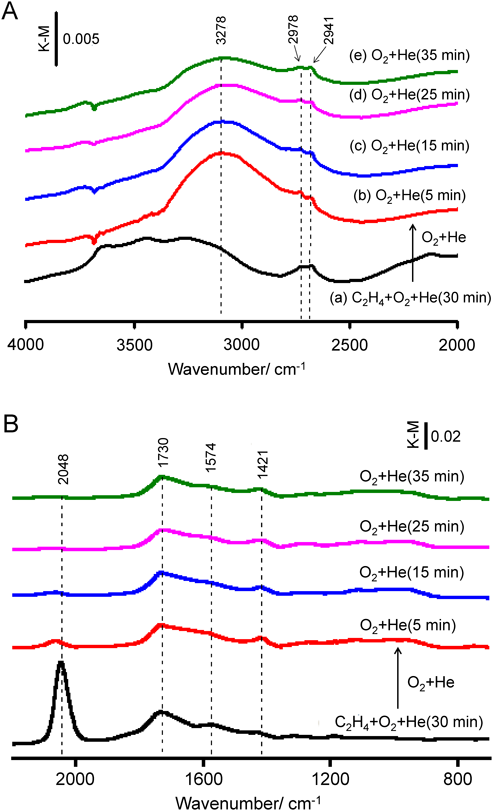
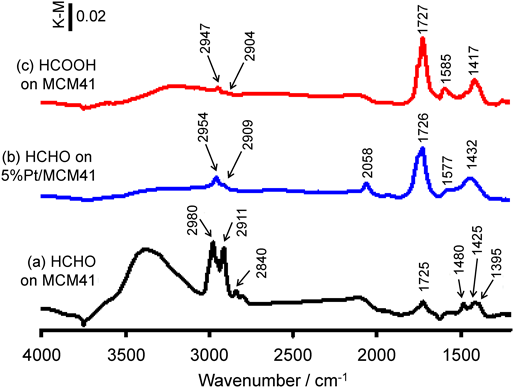
メソポーラスシリカ表面に担持した白金ナノ粒子によるエチレン酸化の反応メカニズムを,フーリエ変換赤外拡散反射(Diffuse Reflectance Infrared Fourier Transform, DRIFT)分光分析によって検討した。水素気流下で200°C, 1時間の前処理をしたPt(5 wt%)/MCM-41に対して,50°Cにてエチレン混合ガス(C2H4 : 0.2 mL min−1, O2 : 4 mL min−1, He : 16 mL min−1)を30分間流通させてIRスペクトルを測定し(図10(a)),さらにその後でエチレンの供給のみを停止して一定間隔にてIRスペクトルを測定した(図10(b)–(e))。図10に示したスペクトルは,ヘリウム雰囲気下で測定したバックグラウンドスペクトルとの差スペクトルである。図10(a)では導入したエチレンに帰属される吸収バンドは見られないが,反応によって形成した水分子(OH伸縮振動,3278 cm−1),ギ酸分子15)(2978 cm−1 : CH伸縮振動,1730 cm−1 : C=O伸縮振動,1421 cm−1 : C–O伸縮振動),ギ酸塩種16)(2941 cm−1 : CH伸縮振動,1574 cm−1 : C–O非対称伸縮振動),および白金に吸着した一酸化炭素8,9)(CO伸縮振動,2048 cm−1)に由来するシグナルが確認された。ギ酸またはギ酸塩の帰属は,参照実験として白金を担持していないMCM-41にギ酸を導入した際に観察されるシグナルに基づいている(図11(c))。試料へのエチレンの導入を止めてヘリウム–酸素混合ガスのみを流通させたときのスペクトル変化(図10(b)–(e))を見ると,CO由来のシグナルは速やかに減少したのに対し,ギ酸およびギ酸エステルに由来するシグナルは35分後でも残存していた。
以上のIR測定に加え,エチレン酸化反応で最初に生成するホルムアルデヒドをプローブに用いた吸着実験を実施し,さらに反応機構の解明を進めた。図11には,MCM-41およびPt/MCM-41に対してホルムアルデヒドを導入したときのFTIRスペクトルを示す。MCM-41にホルムアルデヒドを導入したときのIRスペクトル(図11(a))に見られるシグナルは図10(a)には存在していないため,エチレン酸化反応の中間体と考えられるホルムアルデヒドの生成は直接観察できなかった。注目すべきは,ホルムアルデヒドをPt/MCM-41へ導入したときに得られたIRスペクトル(図11(b))がエチレン酸化反応で得られたIRスペクトル(図10(a))とよく一致していることである。これは,エチレン酸化によって最初に生成するホルムアルデヒドの分解反応が速いためにIR測定では観察できないが,ホルムアルデヒドが白金粒子上で酸化されギ酸(ギ酸塩)または一酸化炭素へと変換される間接的な証拠である。
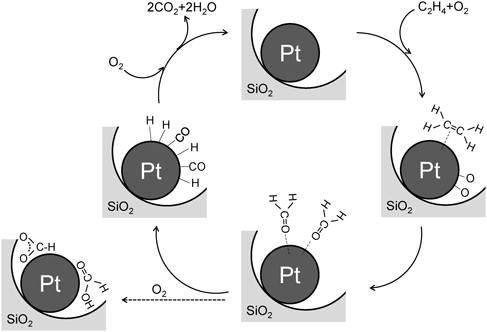
以上の結果から,Pt/MCM-41におけるエチレン酸化反応の推定される反応機構を図12に示す。白金粒子上に吸着したエチレンは原子状酸素と速やかに反応してホルムアルデヒドへと変化する。生成したホルムアルデヒドがさらに酸化されることにより一酸化炭素と原子状水素が生成するが,これらは白金上の原子状酸素と逐次的に反応して二酸化炭素と水に変換される。生成したホルムアルデヒドの一部は並行する副反応によってギ酸へと変換され,それらはメソポーラスシリカ表面でギ酸またはギ酸塩種として安定化される。もう一つの重要な知見は,担持白金触媒の担体効果についてである。他の酸化物担体における反応メカニズムを解析したところ,例えばPt/Al2O3ではC2の酢酸塩の吸着種が観測された。Pt/MCM-41では上述のようにC1のギ酸・ギ酸塩のみが観測されるので,C=C結合が切断されている。従って,Pt/MCM-41の高い触媒活性は,C=C結合の開裂とCO酸化に有利な白金ナノ粒子を高分散担持できるシリカの表面状態と,高い表面積と基質・生成物の拡散に有利なメソ細孔構造をもつことに由来すると考えている。
メソポーラスシリカ担持白金触媒は,0°Cにおいて低濃度エチレンを完全分解できることを見出した。生成した水による活性低下は見られるが,加熱処理によって吸着水を除去すると初期活性が回復して何度も繰り返し使用できる。この高い触媒活性と安定性は冷蔵庫内において野菜・果物から発生する低濃度エチレンの除去技術としても非常に有用であり,実際に実用化触媒として冷蔵庫に搭載された(日立,2015年8月)。この触媒は,メソポーラスシリカを用いた実用化触媒の最初の開発例になったと考えている。これまでに多様な組成・細孔構造をもつメソ多孔体が開発されてきたが,本当の意味で「メソサイズの細孔」と「規則的な配列構造」が寄与した“メソ多孔体でなければ達成できない技術”というのは極めて少ない。本反応系においても,細孔構造の意義は完全には解明されていない。多様な酸化・還元反応に有用なメソポーラス担持金属触媒を開発するためにも,エチレン酸化反応におけるメソポーラス構造の役割を解明することは重要である。本研究が大きく発展することにより,メソ多孔体をベースとして有用な触媒が開発されることを期待している。
謝辞Acknowledgments
最後に実験を行った江川霞博士,横谷卓郎学士,原賢二准教授(東京工科大学)と共同研究を行った太陽化学(株),日立アプライアンス(株)に感謝する。
引用文献References
1) 茶珍和雄,日本食品低温保存学会誌,15, 87–93 (1989).
2) 久保康隆,平田治,稲葉昭次,中村怜之輔,日本食品低温保存学会誌,22, 79–83 (1996).
3) 山下市二,川嶋浩樹,近藤康人,檀和弘,永田雅靖,日本食品低温保存学会誌,22, 191–197 (1996).
4) N. Imanaka, T. Masui, A. Terada, H. Imadzu, Chem. Lett. 37, 42–43 (2008).
5) J. J. Li, C. Y. Ma, X. Y. Xu, J. J. Yu, Z. P. Hao, S. Z. Qiao, Environ. Sci. Technol., 42, 8947–8951 (2008).
6) C. Y. Ma, Z. Mu, J. J. Li, Y. G. Jin, J. Cheng, G. Q. Lu, Z. P. Hao, S. Z. Qiao, J. Am. Chem. Soc., 132, 2608–2613 (2010).
7) W. J. Xue, Y. F. Wang, P. Li, Z. T. Liu, Z. P. Hao, C. Y. Ma, Catal. Commun., 12, 1265–1268 (2011).
8) S. J. Huang, K. Hara, A. Fukuoka, Chem. Eur. J., 18, 4738–4747 (2012).
9) A. Fukuoka, J. Kimura, T. Oshio, Y. Sakamoto, M. Ichikawa, J. Am. Chem. Soc., 129, 10120–10125 (2007).
10) C. Jiang, K. Hara, A. Fukuoka, Angew. Chem. Int. Ed., 52, 6265–6268 (2013).
11) M. Kruk, M. Jaroniec, Chem. Mater., 13, 3169–3183 (2001).
12) J. R. Anderson, Structure of Metallic Catalysts, Academic Press, New York, 1975, pp. 358–363.
13) G. Bergeret, P. Gallezot in Handbook of Heterogeneous Catalysis, Vol. 2 (Eds.: G. Ertl, H. Knçzinger, J. Weitkamp), VCH, Weinheim, 1997, pp. 439–464.
14) M. C. Kung, R. J. Davis, H. H. Kung, J. Phys. Chem. C, 111, 11767–11775 (2007).
15) G. X. Li, M. J. Ridd, F. P. Larkins, Aust. J. Chem., 44, 623–626 (1991).
16) G. J. Millar, C. H. Rochester, K. C. Waugh, J. Catal., 155, 52–58 (1995).