エチレンやプロピレンの低級オレフィンはポリエチレン,ポリプロピレンなどの合成樹脂,有機化学品製造の重要な原料であり,これらの需要量は年々右肩上がりに伸びている。これまで低級オレフィンは主に軽質ナフサのスチームクラッキングにより製造されてきたが,850°C以上の高温を必要とするエネルギー多消費型プロセスであること,生成物組成比を大きく変えることが困難であることから,現行プロセスに比べエネルギー消費量の削減,生成物組成比のコントロールを可能とするプロセス開発が求められている。そこで近年,強酸性,高表面積,規則的細孔構造および高い熱安定性を有するゼオライト触媒を用いたナフサ接触分解反応プロセス開発が着目され,ゼオライト触媒を用いたナフサに含まれる成分の接触分解反応について国内外で多くの研究報告がされている1–8)。
一般に,細孔を有する固体触媒を用いた反応では,バルク流体中の反応物質が先ず触媒外表面に吸着した後,触媒細孔内を拡散し,活性点へ吸着後,反応が進行する。その後,生成物は細孔内を拡散することでバルク流体中へ移動する。よって,拡散速度に比べ反応速度が大きい場合には,触媒粒子内部の反応成分の濃度は均一ではなく,触媒粒子内部の各点において反応速度が異なってくる。特にゼオライトの細孔径は低級炭化水素の分子径と近い値であるため,ゼオライト結晶内の拡散はバルク中の分子の拡散(分子拡散)に比べ非常に遅い。また,ゼオライトの結晶径は細孔径に比べると非常に大きいため,接触分解の反応速度はゼオライト結晶内での反応物や生成物の拡散速度によって制限を受ける場合がある。よって,反応活性,生成物選択性には触媒活性点上での反応速度と反応物,生成物の拡散速度の関係が強く影響する。このため,ゼオライト触媒の活性点上での反応速度とゼオライト結晶内の拡散速度の両面からの触媒設計が重要となる。本解説では,MFI型ゼオライト触媒を用いたナフサ関連物質の接触分解反応の速度解析とThiele数と触媒有効係数を用いた反応工学的触媒設計について紹介する。
2.1 反応次数,反応速度定数の決定9)
MFI型ゼオライト触媒を用いたナフサ留分の接触分解反応には,固定層流通式反応器を用い,475~650°Cの温度領域で実施した。ナフサ留分のモデルとして,n-ヘキサン,シクロヘキサン,メチルシクロヘキサンを用いた。使用したMFI型ゼオライトのSi/Al比は110,150,200,320であり,Si/Al比が200,320のMFI型ゼオライトについては一般的な水熱合成法あるいは水/界面活性剤/有機溶媒を用いたエマルション法により粒径の異なるゼオライトを合成し使用した10,11)。なお,MFI型ゼオライトは粒径に依らずミクロ孔容積,酸点量がほぼ同一であることを確認している。
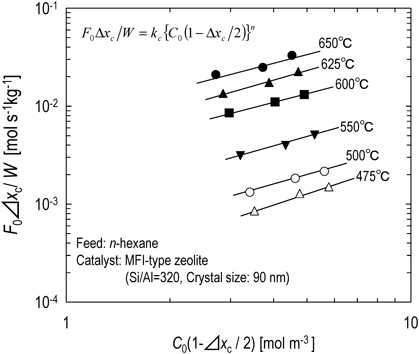
管型反応器を用いた反応では反応速度が原料濃度のn次に比例する場合,反応転化率が低い条件において次の関係式が成り立つ。
ここで,C0, F0はそれぞれ反応器入口での原料濃度,原料供給速度を,kc, W,n, xcはそれぞれ接触分解反応速度定数,触媒重量,反応次数,反応転化率を表している。
図1に一例としてSi/Al=320のMFI型ゼオライトを用い,n-ヘキサン接触分解反応を475~650°Cの温度領域で行った時のF0Δxc/WとC0(1−Δxc/2)の関係を示す。図より各温度において,測定結果は一本の直線で相関された。直線の傾きは反応次数(n)を表しており,各反応温度において直線の傾きは概ね1であった(表1)。これは,n-ヘキサンの接触分解が反応温度に依らずn-ヘキサン濃度に対し1次で進行することを示す。また,MFI型ゼオライトのSi/Al比,原料(シクロヘキサン,メチルシクロヘキサン)に依らず反応次数は1であった。
表1 MFI型ゼオライト(Si/Al=320)を用いたヘキサン接触分解の速度解析より得られた反応次数と反応速度定数| Temperature/°C | Reaction order/— | Rate constant/m3 kg−1s−1 |
|---|
| 475 | 1.2 | 2.5×10−4 |
| 500 | 1.0 | 3.9×10−4 |
| 550 | 1.0 | 9.7×10−4 |
| 600 | 0.9 | 2.8×10−3 |
| 625 | 1.0 | 4.7×10−3 |
| 650 | 0.9 | 7.4×10−3 |
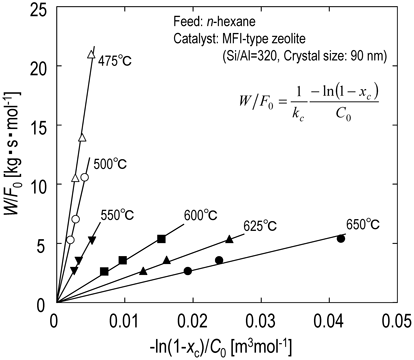
接触分解反応が原料濃度の1次で進行する場合,固体触媒を充填した管型反応器の原料成分の物質収支式は式(2)で表される。
図2はMFI型ゼオライト(Si/Al=320)を用いたn-ヘキサン接触分解反応におけるW/F0と(−ln(1−xc))/C0の関係を示す。いずれの反応温度においても実験結果は原点を通る一本の直線で相関された。ここで図中の傾きの逆数は反応速度定数を表しており,得られた反応速度定数を表1にまとめた。なお,接触分解反応の速度定数導出には,得られた転化率から熱分解の転化率を引いたものを接触分解の転化率として用いた。
2.2 n-ヘキサン,シクロヘキサン,メチルシクロヘキサン接触分解の反応速度定数9,12)
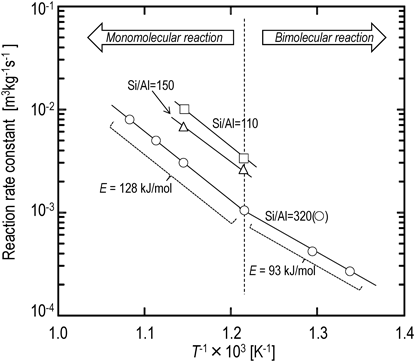
図3はMFI型ゼオライトナノクリスタル(Si/Al=320)を用いたヘキサン接触分解反応速度定数のアレニウスプロットを示す。アレニウスプロットの傾きは550°C~650°Cの高温領域と450°C~550°Cの低温領域で異なり,活性化エネルギーはそれぞれ128 kJ/mol,93 kJ/molであった。これは,高温,低温領域でn-ヘキサン接触分解反応の反応機構が異なるためであると考えられる。Brønsted酸点上でのパラフィンの接触分解反応ではmonomolecular cracking mechanismとbimolecular cracking mechanismの二つの機構が考えられている13)。
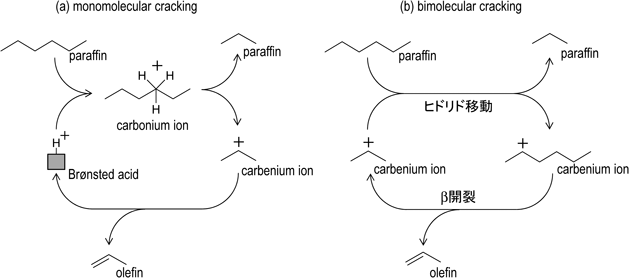
①monomolecular cracking mechanism(図4(a)):Brønsted酸点からパラフィンへのプロトン付加により5配位のカルボニウムイオンが形成される。このカルボニウムイオンからパラフィンあるいは水素分子が生成すると,3配位のカルベニウムイオン中間体が形成される。このカルベニウムイオンからプロトンが移動して酸点が再生され,オレフィンが生成する。
②bimolecular cracking mechanism(図4(b)):低分子カルベニウムイオンに原料のパラフィンがヒドリドを与えることで低分子カルベニウムイオンがパラフィンとなり,原料パラフィン自身はカルベニウムイオンとなる。その後,C–C結合の切断を受けることで低分子のオレフィンとカルベニウムイオンとなり,ここで生成した低分子カルベニウムイオンは,原料パラフィンと反応する。
図3で示した高温領域での活性化エネルギー128 kJ/molは,Haagらが報告したmonomolecular crackingの活性化エネルギー126 kJ/mol13)に近い値であることから,550°C以上の高温領域におけるn-ヘキサン接触分解はmonomolecular crackingが支配的であると推察される。片田らは,490~533°Cの温度でH-ZSM-5を用いたn-ヘキサン接触分解反応の活性化エネルギーは92 kJ/molと報告しており14),低温領域で得られた活性化エネルギーとほぼ等しい値である。また,Haagらはbimolecular crackingの活性化エネルギーはmonomolecular crackingの活性化エネルギーよりも小さい値となることを報告している13)。よって,550°C以下の低温領域におけるヘキサン接触分解反応ではbimolecular crackingも生じていると考えられる。
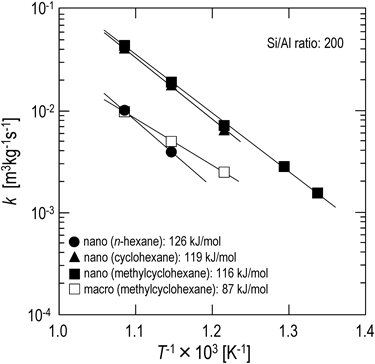
図5はSi/Al比が200のMFI型ゼオライトナノクリスタルを用いたn-ヘキサン,シクロヘキサン,メチルシクロヘキサン接触分解反応の反応速度定数のアレニウスプロットを示す。メチルシクロヘキサンについてはマクロクリスタルを用いた結果も示している。シクロヘキサンおよびメチルシクロヘキサン接触分解の反応速度定数はほぼ等しい値を示し,n-ヘキサン接触分解の速度定数に比べ高い値となった。また活性化エネルギーについては,シクロヘキサン(119 kJ/mol)とメチルシクロヘキサン(116 kJ/mol)ではほぼ等しい値であり,n-ヘキサン(126 kJ/mol)に比べ低い値となった。これより,ナフテンはパラフィンよりも反応性が高いことを示している。一方で,MFI型ゼオライトの結晶サイズに着目すると,MFI型ゼオライトマクロクリスタルを用いたメチルシクロヘキサン接触分解の反応速度定数および活性化エネルギーは,共にナノクリスタルを用いた反応に比べ低い値であった。本解説では結果を示していないが,n-ヘキサンの接触分解反応においても同様にゼオライト結晶径が大きくなると反応速度定数,活性化エネルギーが低下することを確認している9)。詳細については次節で述べる。
ゼオライト触媒を用いたナフサ関連物質接触分解の見かけの反応速度定数は,反応原料(活性点上での真の反応速度)やゼオライト結晶径(結晶内の拡散速度)に影響を受ける。拡散抵抗を受ける反応条件では,原料濃度がゼオライト結晶の外表面から結晶内部にかけて低下するため,ゼオライト結晶内部の原料濃度が不均一となる。これにより,結晶内部の原料濃度が均一な理想的な反応速度に比べ見かけの反応速度は小さい値となる。また,接触分解により得られるC2,C3成分のゼオライト結晶内拡散係数はナフサ留分に比べ大きいが,拡散の遅い成分が共存することでゼオライト結晶内での拡散が制限される15)。これにより,生成物の結晶内での滞留時間が長くなり逐次反応が進行することで,目的生成物収率の低下,コーク生成による活性低下につながると考えられる。そこで,反応律速下で接触分解反応が進行するゼオライト結晶径の検討が重要となる。
MFI型ゼオライトを用いたn-ヘキサン,シクロヘキサン,メチルシクロヘキサン接触分解反応においてゼオライトの結晶径が反応の律速段階に及ぼす影響を明らかにするため,Thiele数(ϕ)と触媒有効係数(η)を用いた検討を行った。MFI型ゼオライトのような平板状であり,反応が1次反応で進行する場合,Thiele数および触媒有効係数はそれぞれ式(3),式(4)で表され,触媒有効係数はThiele数のみの関数として表される16–19)。
ここで,L,ρp, Deffはそれぞれ拡散距離,ゼオライトの見かけ密度,反応物の有効拡散係数である。
Thiele数導出に用いた各反応物の有効拡散係数は,定容法により測定した。ベンゼンを拡散物質とした場合,高い温度領域においてMFI型ゼオライト酸点上での吸着の影響は小さくなり,Alを含まないMFI型ゼオライトであるsilicalite-1を吸着剤に用いた場合の拡散係数とほぼ等しくなることから20),吸着剤にはsilicalite-1を用いた。また,拡散係数測定中の反応を避けるため,測定温度は300°Cで行った21)。
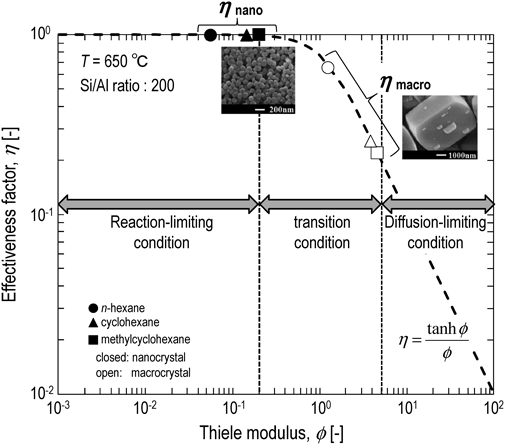
MFI型ゼオライトナノクリスタル(Si/Al=200)を用いた各原料の接触分解反応により得られた反応速度定数と定容法を用いた測定により得られた有効拡散係数を用い,反応温度650°CにおけるThiele数および触媒有効係数の算出を行った。多孔性固体触媒を用いた反応の律速段階はThiele数を用いることで,次の3つに分類される。
- (1)反応律速(ϕ≦0.2)
- (2)遷移領域(0.2<ϕ<5)
- (3)拡散律速(ϕ≧5)
Thiele数が0.2より小さい場合,活性点上での反応速度に比べ拡散速度が大きいため,触媒粒子内部の原料濃度は触媒表面の濃度とほぼ同一であり,粒子内部の活性点のほとんどが反応に活用される。この際,触媒有効係数は0.99以上となり,反応律速下で反応が進行することを表している。一方で,Thiele数が5より大きい時,触媒有効係数は0.2以下となる。反応が迅速に進行するために原料濃度が触媒粒子表面から内部に向けて急激に低下し,粒子表面近傍の狭い範囲(粒子の20%以下)にある活性点で反応が進行しており,拡散律速の状態にある18)。図6は触媒有効係数とThiele数の関係を示している。MFI型ゼオライトナノクリスタルを用いた反応では,原料種に依らず650°Cにおいて触媒有効係数は0.99以上の値をとることから,接触分解反応は反応律速下で進行していると言える。よって,ナノクリスタルを用いて得られた反応速度定数は,拡散の影響を受けない真の反応速度定数であると考えられる。また,式(3)は式(5)のように変形することができ,式(5)にϕ=0.2を代入することで,反応律速下で反応を進行させるためのゼオライト結晶径の最大値を求めることができる。
反応温度650°Cにおいてn-ヘキサン,シクロヘキサン,メチルシクロヘキサン接触分解を反応律速下で進行させるためのMFI型ゼオライト(Si/Al=200)の結晶径はそれぞれ,340, 100, 90 nm以下と算出される。一方,MFI型ゼオライトマクロクリスタルを用いたn-ヘキサン接触分解反応時の触媒有効係数は0.65であるのに対し,ナフテン接触分解反応時の触媒有効係数は約0.2であった。n-ヘキサンの有効拡散係数はナフテンに比べ高い値であることに加え,n-ヘキサンの接触分解反応速度定数はナフテンに比べ小さい値であるため,ナフテンのThiele数はヘキサンより大きい値となる。これは,ナフテンの接触分解反応はゼオライト結晶内の拡散の影響を受けやすいことを示している。また,各反応原料の有効拡散係数は触媒の結晶径に依らず等しいものの,ゼオライト結晶内を拡散する分子の拡散抵抗はL2/Deffで表されるため,拡散距離が長くなるほど拡散抵抗を受けることとなる。例えば,拡散距離が1000 nmのゼオライトは50 nmのゼオライトより拡散抵抗が400倍高いことになる。そのため,MFI型ゼオライトマクロクリスタルを用いた接触分解反応は,ナノクリスタルよりも拡散抵抗が大きく,遷移領域や拡散律速に近い状況下で反応が進行した。
2.2節で,n-ヘキサンやメチルシクロヘキサン接触分解反応の活性化エネルギーはゼオライト結晶径が大きくなることで低下することを示した。これは,ナノクリスタルを用いた場合とマクロクリスタルを用いた場合で反応の律速段階が異なるためである。1次反応で反応が進行する場合,拡散律速下では見かけの活性化エネルギーが真の活性化エネルギーの半分の値になることが知られている。ナノクリスタルを用いたメチルシクロヘキサン接触分解反応は反応律速下で進行し,この時の活性化エネルギーは116 kJ/molであることから,拡散律速下の見かけの活性化エネルギーは58 kJ/molと算出される。マクロクリスタルを用いたメチルシクロヘキサン接触分解反応の活性化エネルギーは87 kJ/molであり,反応律速下と拡散律速下の活性化エネルギーの中間の値である。マクロクリスタルを用いたメチルシクロヘキサンの接触分解反応は反応律速と拡散律速の間の遷移領域で進行しているため,ゼオライト結晶内のメチルシクロヘキサンの拡散が接触分解反応に強く影響し,ナノクリスタルを用いた反応に比べ見かけの反応速度定数,活性化エネルギーが小さい値となった。
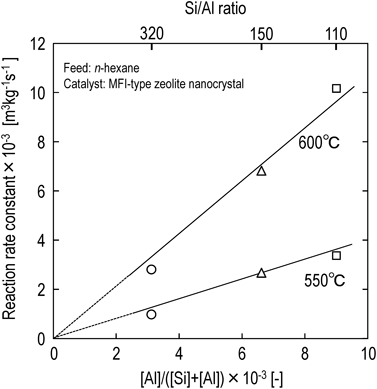
接触分解反応はゼオライトの酸点上で反応が進行するため14),ゼオライトの酸点量つまりゼオライトのSi/Al比が接触分解反応の反応速度定数に影響を及ぼす。図3に示すようにMFI型ゼオライトナノクリスタルのSi/Al比が低くなるにつれてn-ヘキサン接触分解反応の反応速度定数は大きくなっている。図7にMFI型ゼオライトの骨格中のAl量と解析により得られた反応速度定数の関係を示しており,反応速度定数はAl量に対し線形の関係があることがわかる。そこで,次の関係式が得られる。
ここで,[Si],[Al]はゼオライト骨格中のSiとAlの濃度を表している。また,aは図7の傾きであり,550°C,600°Cの傾きはそれぞれ0.38,1.1であった。
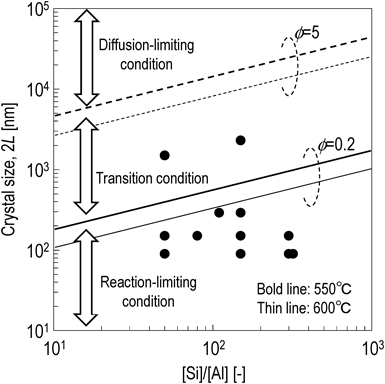
式(5)に式(6)を代入することで,式(7)が得られる。式(7)はゼオライトのSi/Al比とゼオライトの結晶径(2L)の関係を表す式であり,式(7)中のϕ(Thiele数)に0.2あるいは5を代入することで,反応律速(ϕ<0.2)あるいは拡散律速(ϕ>5)となるSi/Al比とゼオライト結晶径(2L)の関係を得ることができる。
図8はMFI型ゼオライトを用いたn-ヘキサン接触分解反応(反応温度:550°C,600°C)におけるSi/Al比と結晶径の関係を示す。反応律速と遷移領域の境界(ϕ=0.2)は実線で,遷移領域と拡散律速の境界(ϕ=5)は点線で示している。図中のプロットはこれまでに筆者らがn-ヘキサン接触分解に用いたMFI型ゼオライトのSi/Al比と結晶径を示している22,23)。詳細な結果は示さないが,結晶径150 nmのMFI型ゼオライトを用いたヘキサン接触分解反応(550°C)において,転化率に違いはあるもののSi/Al比によらず反応中の活性低下は見られなかった。これは反応律速下で反応が進行しているためである。一方で,結晶径がおよそ1500 nmのMFI型ゼオライトでは顕著な活性低下が確認された22)。これは,図8に示される通り反応律速と拡散律速の中間の遷移領域にあり拡散の影響を受けているためである。
本解析結果より,数百ナノメートル以下のMFI型ゼオライトをヘキサン接触分解反応に用いることが反応律速下で反応を進行させるための条件となることがわかる。一方,ゼオライト骨格中のAl量の増加や反応温度の上昇に伴い反応速度定数は高くなるため,反応律速下で反応を進行させるために求められるゼオライト結晶径が小さくなることが明らかとなった。
5. MFI型ゼオライトを用いたモデルナフサの接触分解反応12)
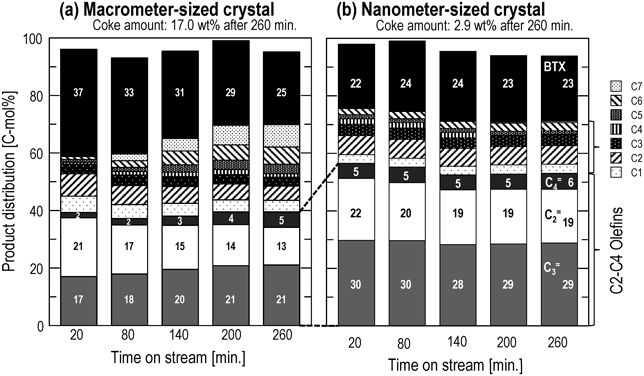
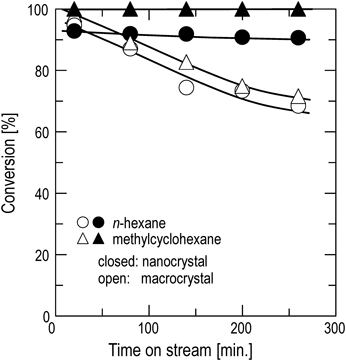
n-ヘキサン,シクロヘキサン,メチルシクロヘキサン接触分解の速度解析から,90 nm以下のMFI型ゼオライトナノクリスタル(Si/Al=200)ではいずれの原料に対しても反応律速下で進行するのに対し,マクロクリスタルの触媒有効係数は低く,特にナフテンについては拡散律速に近い遷移領域で反応が進行することが明らかになった。実際のナフサはパラフィンやナフテン,芳香族の複数の炭化水素成分の混合物である。表2にモデルナフサ組成を示す(既報の値を参考にした24,25))。モデルナフサの主成分はパラフィンであるが,ナフテンやナフテン分子径に近い芳香族が含まれていることから,これらが原料中に共存することでナフサ接触分解中の生成物選択性,触媒寿命に影響すると考えられる。そこで,MFI型ゼオライトマクロクリスタル,ナノクリスタルを用いゼオライトの結晶径がモデルナフサ接触分解に及ぼす影響を検討した。図9および図10は650°Cでモデルナフサ接触分解を行った時の生成物分布およびモデルナフサに含まれるn-ヘキサン,メチルシクロヘキサン転化率の経時変化を示す。
表2 モデルナフサ組成[mol%]| n-hexane | 20 |
| 3-methylpentane | 20 |
| n-heptane | 15 |
| n-octane | 10 |
| cyclohexane | 10 |
| methylcyclohexane | 10 |
| benzene | 5 |
| toluene | 5 |
| xylene | 5 |
マクロクリスタルはナノクリスタルに比べ低いオレフィン収率を示した。さらに,反応時間の経過とともに生成物収率は変化し,n-ヘキサンとメチルシクロヘキサンの転化率は低下した。芳香族(BTX)の生成割合が減少する一方でパラフィンの割合が増加したことから,触媒の劣化が起こっていると考えられる。前述の通りマクロクリスタルを用いたn-ヘキサンやナフテンの接触分解は遷移領域下で反応が進行するため,モデルナフサの接触分解反応は遷移領域あるいは拡散律速下で進行している。複数の成分がゼオライト結晶内を拡散する場合,拡散の遅い成分(ナフテン,芳香族)は拡散の速い成分(直鎖パラフィン,オレフィン)の拡散を阻害する15)。このため,反応により生成したオレフィンは結晶外へ拡散しにくくなり,ゼオライト結晶内での滞留時間が長くなっていると推察される。ゼオライト結晶内でのオレフィンの滞留時間が長くなることで,逐次的な反応が進行しBTXやコークが生成するため,反応終了時のコーク析出量は17.0 wt%と高く,反応中のコーク析出により反応時間の経過とともに活性が低下した。一方で,ナノクリスタルはマクロクリスタルよりも高い低級オレフィン割合,安定した活性を示した。ナノクリスタルを用いたヘキサン,ナフテン接触分解は反応律速下で反応が進行するため,モデルナフサを原料に用いた場合においても反応律速下で反応が進行していると考えられる。また,反応原料,反応生成物の拡散抵抗が小さいためにコーク生成が抑制され,活性の安定につながった。
実際の反応プロセスでは,粉体のまま触媒を充填層反応器に導入すると圧力損失が非常に高くなるため,バインダーを用いた成形体として反応に用いられる。成形体を用いた場合には,原料が成形体のマクロ孔内,ゼオライト結晶内を拡散した後に反応が進行する。成形体触媒の触媒有効係数は,成形体のマクロ孔およびゼオライト結晶ミクロ孔それぞれに由来する触媒有効係数の積で与えられることから,両方の触媒有効係数を考慮する必要がある26)。特にゼオライトは拡散の影響を受けやすく,反応速度,拡散速度に基づく触媒設計が重要である。本報では,MFI型ゼオライト触媒を用いたナフサ関連物質接触分解反応を例に,接触分解反応速度解析とThiele数および触媒有効係数に基づき反応律速を可能とするゼオライト結晶径の推定法について紹介し,数百ナノメートル以下のMFI型ゼオライトナノクリスタルを用いることでナフサ接触分解反応が反応律速下で進行することを示した。また,90 nmのMFI型ゼオライトナノクリスタルはモデルナフサ接触分解反応の活性,生成物選択性の安定化に対し有効であることを示した。ゼオライトのナノサイズ化はゼオライト結晶内での拡散抵抗の低減と逐次反応抑制による生成物選択性の向上,ゼオライト触媒の劣化要因の一つであるコーク析出抑制効果が高いと言える。このように,ゼオライト触媒の反応工学的な触媒設計により,目的とする反応系に対し,触媒結晶径,反応速度や拡散速度に影響する酸強度,酸点分布や細孔構造などの設計指針が得られると期待される。
一方で,コーク析出を完全に抑えることは困難であり長期的な利用を考えればコーク析出による活性低下を避けることは難しい。反応中のコーク析出位置27,28)や反応速度,拡散速度に基づいたコーク析出による触媒の劣化機構21,29,30)に関する報告は最近いくつか有るものの情報が少ない。反応速度や拡散機構の解析に基づいたコーク析出による触媒劣化機構を明らかにしていきたい。
謝辞Acknowledgments
本研究は,独立行政法人新エネルギー・産業技術総合開発機構(NEDO)の委託業務(平成21~25年)として行われたものである。
引用文献References
1) A. Corma, J. Mengual, P.J. Miguel, Appl. Catal. A: Gen., 460–461, 106 (2013).
2) Y.V. Kissin, J. Catal., 163, 50 (1996).
3) H. Mochizuki, T. Yokoi, H. Imai, R. Watanabe, S. Namba, J.N. Kondo, T. Tatsumi, Micropor. Mesopor. Mater. , 145, 165 (2011).
4) A. Corma, J. Mengual, P.J. Miguel, Appl. Catal. A: Gen., 421, 121 (2012).
5) A. Yamaguchi, D. Jin, T. Ikeda, K. Sato, N. Hiyoshi, T. Hanaoka, F. Mizukami, M. Shirai, Fuel Proc. Technol., 126, 343 (2014).
6) S. Inagaki, K. Takechi, Y. Kubota, Chem. Commun., 46, 2662 (2010).
7) K. Kubo, H. Iida, S. Namba, A. Igarashi, Micropor. Mesopor. Mater., 149, 126 (2012).
8) K. Urata, S. Furukawa, T. Komatsu, Appl. Catal. A: Gen., 475, 335(2014)
9) Y. Nakasaka, T. Okamura, H. Konno, T. Tago, T. Masuda, Micropor Mesopor. Mater., 182, 244 (2013).
10) T. Tago, M. Nishi, Y. Kouno, T. Masuda, Chem. Lett., 33, 1040 (2004).
11) T. Tago, K. Iwakai, M. Nishi, T. Masuda, J. Nanosci. Nanotechnol., 9, 612 (2009).
12) H. Konno, R. Ohnaka, J. Nishimura, T. Tago, Y. Nakasaka, T. Masuda, Catal. Sci. Technol., 4, 4265 (2014).
13) W.O. Haag, R.M. Desau, R.M. Lago, Stud. Surf. Sci. Catal., 60, 255 (1991).
14) N. Katada, K. Suzuki, T. Noda, W. Miyatani, F. Taniguchi, M. Niwa, Appl. Catal. A: Gen., 373, 208 (2010).
15) T. Masuda, Y. Fujikata, H. Ikeda, K. Hashimoto, Micropor. Mesopor. Mater., 38, 323 (2000).
16) E.W. Thiele, Ind. Eng. Chem., 31, 916 (1939).
17) R. Aris, Ind. Eng. Chem. Fundam., 4, 227 (1965).
18) O. Levenspiel, Chemical Reaction Engineering, John Wiley & Sons, 2nd edn, 1972, p.460.
19) H. F. Fogler, Elements of Chemical Reaction Engineering, Prentice Hall, 4th edn, 2006, p.813.
20) T. Masuda, Catal. Surv. Asia, 7, 133 (2003).
21) Y. Nakasaka, J. Nishimura, T. Tago, T. Masuda, Chem. Eng. J., in press.
22) H. Konno, T. Okamura, Y. Nakasaka, T. Tago, T. Masuda, J. Jpn. Petrol. Inst., 55, 267 (2012).
23) H. Konno, T. Tago, Y. Nakasaka, R. Ohnaka, J. Nishimura, T. Masuda, Micropor. Mesopore. Mater., 175, 25 (2013).
24) A. Juarez and V. Macias, Energy Fuels, 14, 1032 (2000).
25) S.Y. Han, C.W. Lee, J.R. Kim, N.S. Han, W.C. Choi, C.H. Shin, Y. K. Park, Stud. Surf. Sci. Catal., 153, 157 (2004).
26) T. Masuda, J. Jpn. Petrol. Inst., 46, 281 (2003).
27) L. Pinard, S.Hamieh, C. Canaff, F.F. Madeira, I. Batonneau-Gener, S. Maury, O. Delpoux, K.B. Tayeb, Y. Pouilloux, H. Vezin, J. Catal., 299, 284 (2013).
28) L. Pinard, K.B. Tayeb, S. Hamieh, H. Vezin, C. Canaff, S. Maury, O. Delpoux, Y. Pouilloux, Catal. Today, 218–219, 57 (2013).
29) T. Masuda, N. Murakami, K. Hashimoto, Chem. Eng. Sci., 47, 2775 (1992).
30) H.G. Karge, W. Nieben, H. Bludau, Appl. Catal. A: Gen., 146, 339 (1996).