アジア諸国のモータリゼーションの急速な発展に伴い,資源・環境・エネルギー対策は焦眉の急を要する。筆者の世代でも,お隣り中国・天安門広場前の自転車で行き交う人々のイメージが記憶に新しく,昨今の自動車排ガスによる大気汚染状況悪化のニュースや町中の渋滞の様子を伝える映像には隔世の感がある。インドを始め二輪車が多数派であった東南アジア諸国においても目の当たりにした現実の車社会は,今後の環境触媒=自動車触媒システムなどの発展のモチベーションとなっている。
二酸化炭素排出削減に関わって,現在ディーゼル車が再び注目されるようになった。日本では環境悪玉の印象が拭い切れていないが,世界的に期待される内燃機関の自動車である。その日本ではクリーンディーゼル車として,脚光を浴びようとしている。クリーンディーゼル車の排気ガス浄化には,ガソリン車の現行の三元触媒システムが適用できず,新しい触媒システムが開発され続けてきた。時代を追って酸化触媒,PMフィルター,尿素による窒素酸化物還元触媒,アンモニアスリップ用酸化触媒,と多段化され,今の触媒システムが構築された。こと窒素酸化物の除去に関しては,主にバス,トラックなどの重量車両に対して,尿素の加水分解により生成したアンモニアにより窒素酸化物を還元除去する方式が採用されている。この触媒として,銅をイオン交換したSSZ-13ゼオライトをはじめ,多くのゼオライト担持銅あるいは鉄触媒が利用検討され,一部実用化に至っている。再びゼオライト触媒が輝ける時代の到来である。
そのような期待感の中で,果たしてこれまでどの程度,ゼオライトが自動車触媒に対して効果的な役割を果たしてきたのであろうか。筆者がこれまで関わってきた共同研究等の成果を中心に,その関連研究を紹介し,いま現在筆者らが考える“よりよき解”について考察する。本稿をお読みくださる方々の議論の種にでもなれば幸いである。
1950年頃,北米都市部で発生した大規模かつ深刻な大気汚染の原因として,当時の検証の結果から自動車の排気ガスが挙げられた。以降,世界一厳しいと言われたマスキー法の制定が大気汚染対策の飛躍的な進歩につながったとみることができる。マスキー法は実効されなかったとはいえ,自動車触媒技術が学術的にも興味深く進歩し続けられる礎を構築した実績は誰もが認めるであろう。
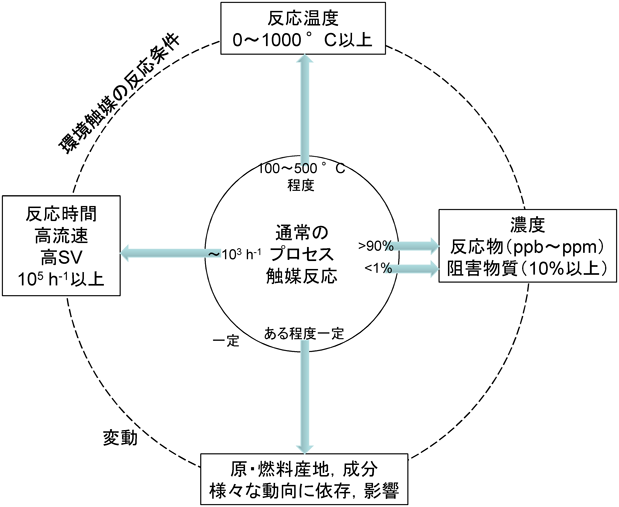
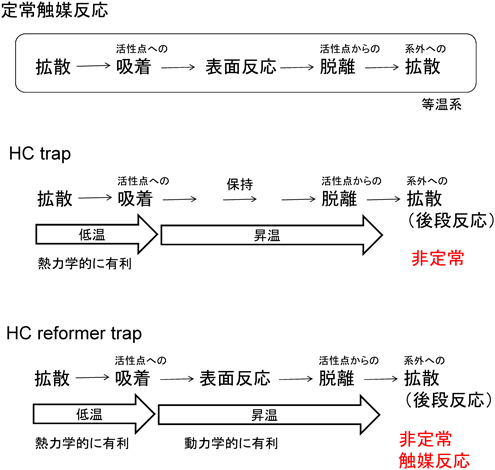
自動車触媒,いわゆる「環境触媒」が如何に難しい触媒プロセスであるか。筆者は講義などでしばしば,東京大学名誉教授の御園生誠先生が図示されたもの1)(図1には筆者が加筆したものを示す)を使って説明する。内側円で表される通常の触媒プロセスとは大きく異なり,反応対象物質の濃度に比べて反応阻害性物質の濃度が100倍程度も高い。適用温度あるいは対処しなければならない温度範囲が極めて広い。接触時間が100 h−1以上短い。これらが時々刻々変動する。つまり,外側点線円で表される触媒適応範囲の位置すら定まっていない。以上の点が,環境触媒を難しいものとしている。
自動車触媒は,基本的には燃焼排ガスを熱源として,除去対象物質に対する各反応の活性化エネルギーを賄っている。いくら優れた触媒とはいえ,室温(場所によって大きく違うが)付近で酸化反応を促進できるようなスーパー触媒はそれほどはない。しかし,自動車排ガスに含まれる未燃炭化水素HCは,エンジン始動時から数十秒間,触媒が排ガスで温められ活性化される前に総量の7, 8割が排出される2)。これがすなわちコールドスタート時のHC排出問題である。この課題解決が光化学スモッグ汚染対策の決め手になる。
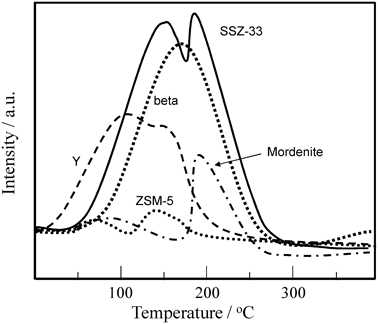
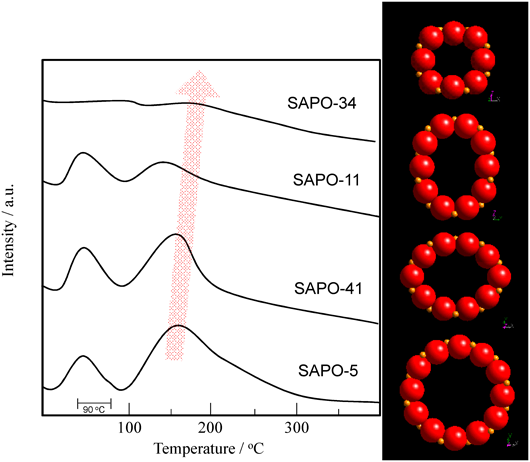
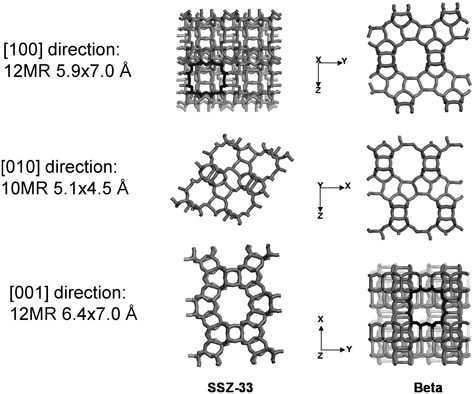
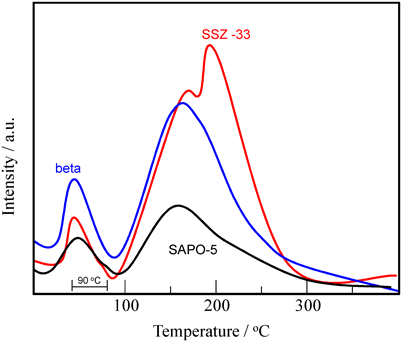
このコールドスタート時の排出HCを吸着して貯蔵し,排ガス温度の上昇に伴い吸着HCを自発的に脱離させ,すでに活性化された後続の三元触媒Three-Way Catalyst: TWCへ供給するHCトラップ方式の浄化システムが採用された。HCに親和性を示すゼオライトがこの吸着材候補として挙げられ,様々なハイシリカゼオライトがテストされた3–7)。自動車排ガス処理触媒の前段に位置し,より高度な水熱安定性が求められるため,ハイシリカゼオライトが検討の中心だったようである。だんだんと上昇する排ガス温度によりTWCが活性化されるまで「時間稼ぎ」することが,本ゼオライト吸着材に求められる本質である。その指標として200°C程度までHCを多量に保持することがHCトラップの必要条件となった。我々も様々なゼオライトを検討し,ベータゼオライトが候補として優れていること(図2),ゼオライト細孔サイズにより有効な炭化水素成分が異なること,細孔サイズが大きいほど吸着量に優れ,小さいほど保持力に優れたゼオライト吸着材となり得ること,などを提案した8)。図3には,本システム検討のHC標準物質であるトルエンを用いて,SAPOの細孔径のみを変化させたときのトルエンTPDプロファイルを示している。いずれもSAPOを用いているため,表面吸着特性は同等と考えている。非常に恣意的に矢印を引いてあるが,細孔径が大きいとトルエン吸蔵容量が大きく,細孔径が小さいと脱離スペクトルが高温までテーリングしている様子がうかがえるであろう。そのような検討をしている最中,当時の研究室ボスである大久保達也助教授(当時)がMark Davis教授より提案され提供を受けたSSZ-33というゼオライトを試してみた。当時としてはたいへん珍しく,酸素12員環細孔と酸素10員環細孔が結晶内部で交差する異径細孔系ゼオライト(図4)であったが,すでに石油化学系触媒として特異性を示すといった報告がなされていた。そこで,上記同様トルエンTPDを用いてHCトラップ性能を評価したところ,図5に示すような興味深いプロファイルが描けることがわかった。ベータゼオライトを用いてもこうなる場合があるが,トルエンの高温側脱離ピークがふたつに分裂すること,前者(分裂ピークの低温側)は12員環ゼオライトのものと脱離温度が極めて近いこと,また後者(高温側)は10員環のそれと近いこと,であった。この様子から,「穴に入らせやすく,穴から出しにくい」molecular traffic controlが起きているのではないかと想像している9)。熱力学的に矛盾無く説明するためには,framework(あるいは細孔内)Al分布の解明が不可欠だと認識している。しかし,同様な細孔システムを有するMCM-68(12×10×10員環の細孔システム)でも効果的にHC脱離を遅らせることが可能であった10)ことから,そんなに過大妄想ではないであろうと期待はしている。
とにかく当時は(現在も?)ゼオライトの自動車触媒としての絶対必須条件は高水熱安定性であったが,SSZ-33は実験室での水熱試験程度ではそのミクロ細孔特性はほぼ失われないことを確認した(表1)9)。このような新しいタイプのゼオライトが適用可能な応用分野が,我々が知らないだけで,まだまだ存在する,と期待を大きく持てた。
表1 HCトラップに適用したゼオライトの物理化学的特性| ゼオライトHCトラップ材 | BET表面積 m2/g | 細孔容積 cm3/g |
|---|
| ベータ(Si/Al=55) | 650 | 0.43 |
| 水熱処理後 | 490 | 0.35 |
| SAPO-5 | 235 | 0.16 |
| 水熱処理後 | 25 | 0.06 |
| SSZ-33 | 615 | 0.48 |
| 水熱処理後 | 570 | 0.47 |
炭化水素吸着・濃縮を利用した反応型HCトラップ=HC reformer trapの提案
HCトラップは「時間稼ぎ」としては素晴らしいシステムである。十分な反応速度あるいは反応の活性化エネルギーを賄うには低いと考えられる温度では,熱力学的に低温有利な吸着を利用しHC回収をおこなっている。しかし,沸点が約110°Cのトルエンを200°C以上にまで吸着保持するためには,ゼオライトの細孔構造や酸点の寄与だけでは限界がある。ナトリウム型ゼオライトを利用するなど,イオン交換サイトにアルカリカチオンを担持することで高温までのトルエン保持が可能であるといった報告例11)があるが,共存する水蒸気の影響を考慮するとベストな方法であるとは言い切れない。またそもそも,吸着されたHCを排ガス温度上昇に伴い脱離させるだけでは,後続のTWCの負担に変わりはなく,たとえばTWCの貴金属使用量低減など,元素戦略の観点からのメリットはない。
我々はここで,HCトラップシステムにもう一度,表面機能を賦活することを提案した(図6)。すなわち,ゼオライトのミクロ細孔内にHCは濃縮されているので,HCを改質する等の表面反応は動力学的に有利となる。TWCのライトオフ温度を考慮して200°Cまでの保持能力が求められているため,改質されたHCが元のHCよりも反応性に富む分子であれば,200°Cまで「時間稼ぎ」しなくても酸化除去されるではないか! もしくは,改質HCの高い反応性ゆえに貴金属触媒の負担が軽減され,貴金属の使用量が低減可能なのではないか?と考察したところからの提言である。
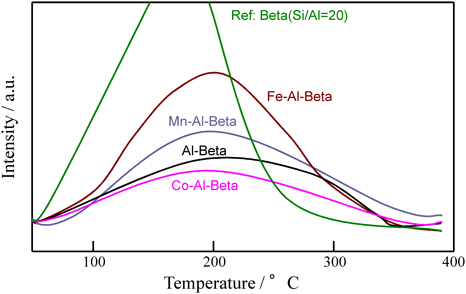
その目的遂行のため,ゼオライト酸点による吸着機能の他に,Redox可能な金属サイトをゼオライトミクロ細孔内に併設し,酸化機能の賦活を試みた。図7には,鉄,マンガン,コバルトなどを担持したベータゼオライトでトルエンTPDを行った際の脱離プロファイルを示す。ここで使用しているAl-betaを始め金属担持されたベータゼオライトはすべて,メソポーラスシリカ・アルミナ+金属酸化物を原料にした固相反応法によって結晶化せしめたものである12)。市販のベータゼオライトに比べて,本法で合成された金属担持ベータゼオライトは温度幅の広い脱離プロファイルを有することがわかる。この段階で,200°C以上の脱離が総脱離量の50%となっているため,保持力はHCトラップとして合格ではある。本実験目的はその脱離HCの成分分析であるので,脱離ガスを各温度で吸引採取し,ガスクロマトグラフにて成分分析をおこなった。すると,非常にわずかではあったが,改質成分(このときはベンズアルデヒドと同定された)が検出されることがわかった13)。共同研究先の自動車会社でも模擬排ガス試験を行ったところ,TWC後方のコールドスタートHC排出量が通常のHCトラップ(プロトン型ベータゼオライト)を利用したシステムと比較して減少することを確認できた。これは理想的には,部分改質されトラップから放出されたHCがコールドスタート低温域でもTWCで酸化除去されたと考えることができる。
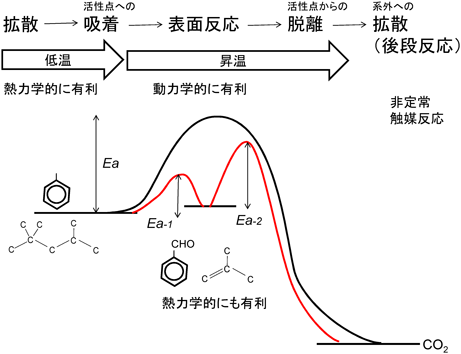
HC reformer trapとは何だったのか? を考えると,実は非定常的な触媒反応プロセスであることに気が付く。トルエン酸化を想定した場合には,通常越えなければならない活性化エネルギーEaに対して,活性中間体(前述の検討では部分酸化物)を与えるようなルートを提供するのがHC reformer trapである。その活性中間体を経て最終酸化生成物CO2にまで酸化されるルートの活性化エネルギーはEa−1,Ea−2となり,Ea>Ea−1, Ea−2が成立する場合にはHC reformer trapがシステムとして成立するのである(図8)。活性中間体を経るルートを与える意味において,まさに触媒の役割そのものである。トルエンを代表的なコールドスタートHC成分(オレフィン,芳香族)として検討する例が多く報告されているが,パラフィン系HCでは2,2,4-トリメチルペンタン(イソオクタン)がガソリン排ガス中でもっとも多く排出される。同様にHC reformer trap特性を評価したところ,放出時にプロトン型ゼオライトでイソブタンとイソブテンに分解できることがわかり,イソブテンがイソオクタンよりも酸化されやすいことからHC reformer trap性が成立することも明らかにすることができた13)。
現在も本検討を続けている。いまは,どうせ改質するのなら,吸着濃縮されたHCをCO2まで完全酸化して放出することができないかと考えている。そこまでいけば,少なくともコールドスタート時のHCには何も憂慮がなくなる訳である。極めて限定的なゼオライトを使うことで,この完全酸化版HC reformer trapが達成しつつある。この件については,いずれどこかで報告できることと思う。
NO吸着濃縮+分解エネルギー印加による二段階NO直接分解
さて,問題は一酸化窒素NOである。HC,一酸化炭素CO,ディーゼル煤Particulate Matter: PMなどの「酸化」除去については,これまでも多くの検討がなされ,触媒の指針が明確化されつつある。一方NOについては,化学量論域でのHC, COとの「還元」反応,酸素過剰条件でのHC-SCR(Selective Catalytic Reduction: 選択的「還元」反応)といった反応が適用され,あるいは多くの研究がなされてきた。HC-SCRについてはごく一部で限定的に実用化されたと聞いているが,TWCに匹敵する技術にはいまだなり得ていない。さらにはTWCは,ディーゼル排ガスなどの酸素過剰条件ではNOを選択的に還元することができず,非選択的還元法とも称される。
窒素酸化物の固定発生源対策として,アンモニアを還元剤としたSCRが可能であり実用されている。一方アンモニアの毒性のため,車載は困難であると判断されている。最近になり,欧州を中心に,バス,トラックなど大型のディーゼル自動車などの移動発生源対策として,尿素によるSCRが実用化されている。尿素を水蒸気と反応させるとアンモニアを生成させることができるため,アンモニアよりは毒性の低い尿素水をタンクで車載し,排ガス流路途中で噴霧添加してオンボードでアンモニアを生成させるシステムである。したがって,本質的にはアンモニアSCRが移動発生源にも適用されたとみなせる。これで万事解決ではなく,スリップアンモニア対策,尿素タンク積載による重量化,など大型排ガス浄化システムが必須となっている。これは大型自動車でなら可能であるが,日本で流行している軽自動車,小型車にはとても難しい。NOは,構成要素を考慮しても直接的に分解して窒素,酸素にすることが一番の理想的な除去の形であろう。しかしこの反応は,いまだに夢の触媒として認知される反応である。
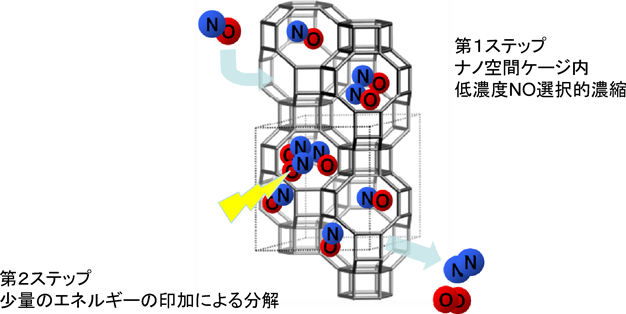
我々はHC reformer trapの成功を機に,非定常触媒反応の実現が必要であろうと考え,二段階に反応を進行させる触媒システムを考案した(図9)。すなわち,
- (1)NOの選択的な吸着濃縮
- (2)反応エネルギーの印加による分解
である。まずは(1)に関して検討を始めた。
吸着サイトには,NO配位に有利な遷移金属系で,なおかつ車載性も考慮し,鉄イオンをイオン交換担持することとした。鉄イオンは通常Fe2+,Fe3+がゼオライト中に安定に存在し得る。Fe2+イオンが酸素共存下においてもNOを選択的に吸着できる能力は,ヘモグロビン中のヘム鉄(Fe2+)が酸素吸着中心となっていることから想像した。一酸化炭素中毒現象は,大気中に21%の濃度をもつ酸素でも数十~数百ppmの一酸化炭素によってヘモグロビンへの酸素吸着が阻害され,血中(脳内)酸素濃度が低下するものである。すなわち,酸素過剰条件においても一酸化炭素を選択的に強吸着する能力が,Fe2+にはあるものと考えられる。そのFe2+は,硫酸塩を使い,水溶液中からゼオライトにイオン交換担持している。硫酸塩はFe2+による青々とした呈色がみられるが,水溶液中に溶解させしばらく時間が経過すると,茶色く変色する。これは溶存酸素によりFe2+がFe3+に酸化されていることを示す。つまり,Fe2+は配位子によって錯化していれば,酸素による酸化作用を受けづらくなり,安定に存在し得ることを意味する。想定通り,ゼオライトにイオン交換担持されたFe2+は青く呈色し,焼成などのポスト処理中でも青く安定に存在していることが確認された。ただし,イオン交換操作中の水溶液中の水和Fe2+イオンは酸化されやすいため,酸化防止剤としてアスコルビン酸をイオン交換溶液に共存させている。また,Fe2+の定量には水素TPRを利用し,Fe全担持量から酸化物,Fe3+を区別することでFe2+担持量を算出していることに注意していただきたい。
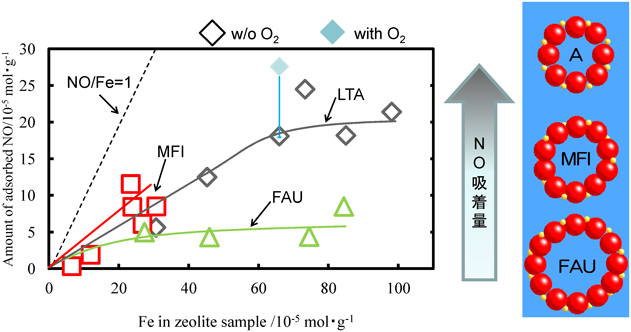
図10には,最も典型的なゼオライトにFe2+をイオン交換担持したサンプルで,NO吸着に対するFe量依存性を示す。FAU,MFI,LTAとSi/Al比が異なるため,Fe2+交換容量に差はあるものの,以下のような傾向を読み取ることができると考えている。すなわち,FAUはFe量を増大させてもNO吸着量が低い値で飽和した。MFIはハイシリカ(Si/Al=12,東ソー製)であるがゆえに,Fe交換量とともにNO吸着量が増大するものの,Fe交換量が低いレベルから伸長しなかった。それらと比べると,LTAはFe交換容量が大きく,かつテストしたサンプルの中では大きいNO吸着容量を示すことがわかる。この段階で,細孔径が小さくなるにつれてNO吸着容量が増大している傾向にあると予想されたが,科学的な説明や根拠に乏しかった。一方注目すべきは酸素共存下でのNO吸着試験であり,酸素共存させてもNO吸着容量にほとんど変化が見られなかった。またFe3+をイオン交換担持したLTAゼオライトにはNO吸着能はほぼみられなかった。このことは,ゼオライトに対して3価の多価カチオンがイオン交換されにくく,NOを吸着しない酸化鉄の形で担持された可能性と,本質的にFe3+にNOが吸着しない可能性と,まだ両面考えられる。ただし,Fe3+にNO2が吸着される報告は比較的数多くある14)。
以上のように,配位不飽和な金属多価カチオンは分子選択的吸着サイトの候補として優れているとみなせる。一方,多価カチオンを安定に固体に保持することがゼオライトの重要な役割のひとつとなってくる。ハイシリカゼオライトでは多価カチオンを細孔内の極めてローカルな位置に固定することは難しい。そこで,LTAのようなアルミニウム量が多く,かつ水熱安定性に優れるという相反する性能をもつゼオライトが必要不可欠となってくる。
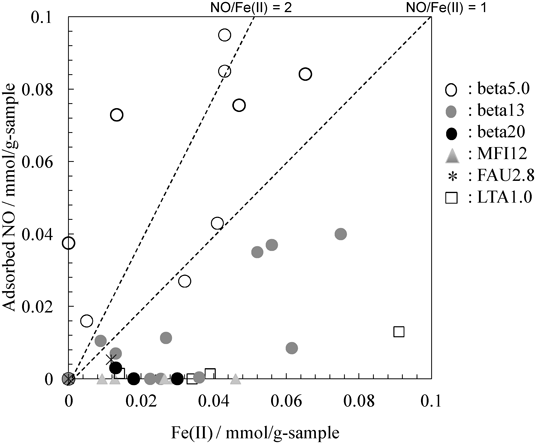
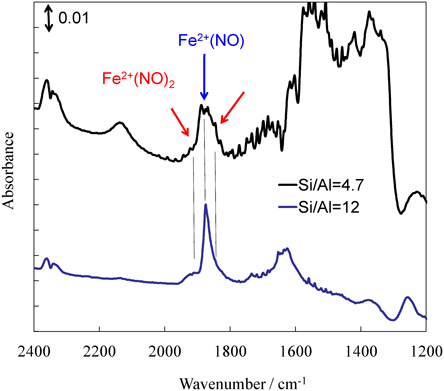
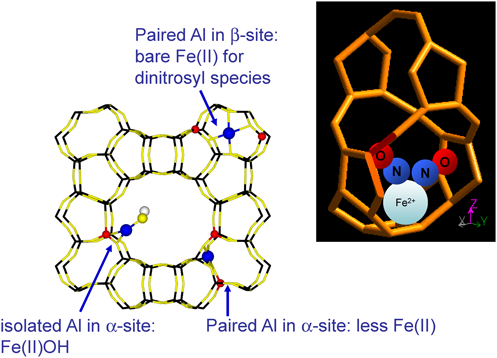
板橋,大久保らの合成するOSDAフリーゼオライトはその有力候補のひとつとなった。詳細は総説などに譲る15)が,本合成系で得られるゼオライトは骨格内Alを多くもつハイアルミゼオライトであること,それにも関わらず水熱安定性に優れていること,が少なくとも我々のニーズに合致していた。市販のベータゼオライト(Si/Al=13, 20),典型的なゼオライトと比較したFe2+ゼオライトのNO吸着容量を纏めた図11を示す16)。さきほど図10で説明していたMFI, LTAなどはNO/ Fe2+モル比が1すなわち単座吸着には程遠い値を示しており,これを吸着効率と称するならばその効率は著しく低いゼオライトと考えることができる。興味深いことに,それらと比較してベータゼオライトは吸着効率が著しく高いことがわかる。一方,Si/Al=20の市販ベータゼオライトでは,Fe2+がゼオライト内に存在するにも関わらず,NOをまったく吸着することができない。Si/Al比の低下に従って,すなわち骨格Al量の増加に伴いNO吸着効率が増加し,NO/Fe2+=1の単座吸着を超えて,NO/Fe2+=2をも超えるような結果を示した。赤外吸収スペクトルで吸着NOの様子を観察する(図12)と,NO吸着種に由来する吸収バンドの半値幅が異なることがわかり,ハイシリカゼオライトの場合であれば狭く,ハイアルミゼオライトでは幅広くなっていることに気がつく。これは,Fe2+に対するモノニトロシル吸着種を吸収帯の中心として,その低波数側と高波数側にそろってジニトロシル種由来の吸収が観察されることを意味している。ハイアルミゼオライトでは,どうやら,Fe2+に対してジニトロシル吸着種が存在しているようだ。このことが,Fe2+ひとつに対するNO吸着個数の増大,つまり吸着効率の良さを表しているのではないか。ハイアルミゼオライトに担持されたFe2+の配位不飽和性が高いということは,つまりFe2+はゼオライト骨格の負電荷のみによって電荷補償されていることを示す。ハイシリカゼオライトの場合には,負電荷がカチオンによって補償可能な距離からさらに離れて存在するため,多価カチオン上にOH−などを配位して電荷補償されていることになり,配位不飽和性が失われている。チェコのグループとの共同研究から,Fe2+はアルミニウム近傍のβサイトに多く存在していることもわかった(図13)16)。
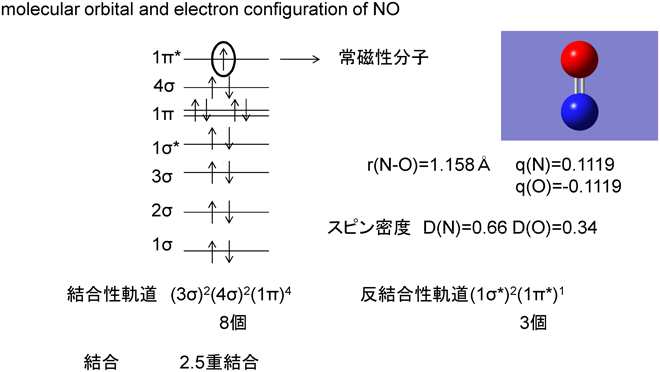
ジニトロシル種としてNOを吸着させることがどのような意味をもつのか。この吸着種から分解へと進む反応経路を探るために,DFT理論を導入して評価を進めることにした17)。まずは基本のおさらいとなるが,NO分子の軌道について説明する。図14に示すようにNOは1π*反結合性軌道に電子ひとつを有する2.5重結合をもつ分子として知られ,その電子を奪う(NO+)ことにより結合長が短くなり結合が安定化する一方,電子を注入する(NO−)ことができれば反結合性軌道に入ることになり,結合長が伸び分子(N–O原子間結合)がさらに不安定化して切断しやすくなる。したがって,NO分子のMulliken chargeを検討することで,NO分子切断触媒としての可能性を評価することにした。
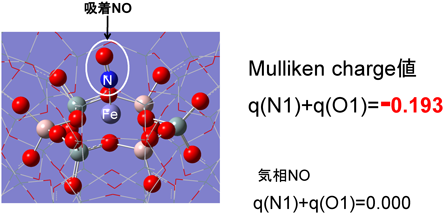
まずはNO伸縮振動のDFT理論計算により,本評価手法の妥当性を検証した。実験値(Fe-ZSM-5上のNO吸着種赤外吸収スペクトル)とほぼ一致したことから,本系の妥当性を確認した。次に,モノニトロシル吸着種をFe-ZSM-5上に構築し(図15), Mulliken chargeを見積もると,q(N)+q(O)=−0.193と算出された。気相NO分子では本値がゼロとなることからも,NO分子そのものが吸着により負に帯電することが明らかとなった。これは,Fe2+からの電子のバックドネーションによるものであると推定できる。
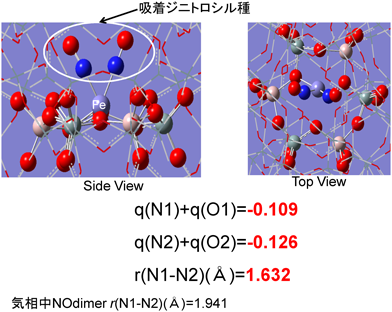
次にジニトロシル種をFe-ZSM-5細孔内に構築し,Mulliken chargeを同様に計算した(図16)。一分子目のNO(−0.109),二分子目のNO(−0.126)ともに負に帯電した。さらには,二分子間距離をN–N間距離で見積もると1.632 Åとなり,気相でNO二量体を形成したときの再安定化距離(1.941 Å)よりも短くなることが示された。NO二分子が同一のFe2+イオン上に吸着されることで,二分子ともにN–O間結合が切れやすい負に帯電した状態になり,N–N間距離が著しく短縮されることが明らかである。
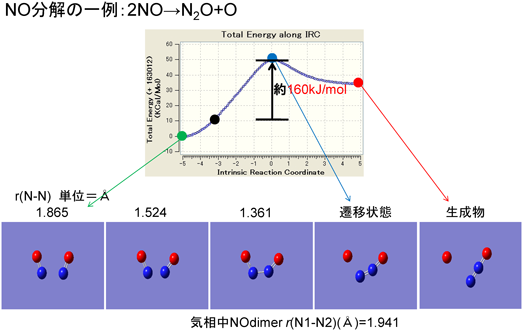
N–N間距離が短くなることの意味は何か。図17にはNO二分子が分解して一次生成物であるN2Oとなる反応パスの活性化エネルギーを示す。NOは二分子ともN側からFe2+上へ吸着され,N–N間距離が縮まることで極大点(図中青いプロット)を通過するのに必要な障壁,つまり活性化エネルギーが小さくなることを意味している。現在のジニトロシル種は黒プロットの位置に相当するため,本反応が起こるためには約160 kJ/molのエネルギー印加が必要となることを表している。つまり,N–N間距離が短くなると,分解反応の活性化エネルギーは小さくなるわけである。また,N2O生成過程がN2,O2まで分解が進行する律速段階となっていることも明らかとなった17)。これらのことから,ゼオライトにイオン交換されたFe2+上に,NO吸着効率の観点からも高効率なジニトロシル種を形成することができれば,直接分解を比較的容易に起こしやすくすることが可能となる。そのためのミクロ孔内選択吸着・濃縮作用が有効になると考えられる。ただし,さらに活性化エネルギーを低下させるためには,さらにN–N間距離を短縮することが求められる。その方法論については現在もまだ検討中である17)。
次は(2)反応エネルギーの印加による分解である。現在この段階についてはマイクロ波(MW)加熱を利用した検討をおこなっている。定性的な解釈として,MWによる急速加熱を利用することで,細孔内に吸着濃縮されたNO分子が脱離する前に分解反応を起こすことができた18)。先に述べたように,Fe-ゼオライトでは酸素過剰共存下でもNOを選択的に吸着させることができる。MWのエネルギーを変化させることで加熱量が可変であり,Cu-ゼオライトでは律速となっている酸素の脱離を促すことでさえ可能となる。また,瞬間加熱では長時間高温に曝されることがなくなるため,ゼオライトだけに留まらず触媒には有利な方法と言える。印加エネルギーのうちどの程度が反応に使用されているのか,電気加熱よりもエネルギー効率が良いと本当に言えるか,分解生成物のN2O/N2選択性などに対する影響,など明らかにしなければならない課題が多く,近い将来報告するので議論していただきたい。
我々はこれらの研究を通じて,ゼオライトの特性を真に引き出し,新しい自動車排ガス浄化触媒をシステムとして考案することを試み,一部実証してきたと考えている。今後ますます厳しくなる規制をクリアするために,環境問題に対して,貧資源国である我々日本人でも適用可能であり,かつエネルギー的観点を考慮し,その時代に合わせたベストな解を提示していきたいと願っている。そのためには今回提案したような「非定常」「配位不飽和な多価金属イオンを安定的に保持するためのハイアルミゼオライト」「細孔内濃縮」「水熱安定性」がいずれもキーワードとなってくると思われる。まったくの私見であるが,触媒を反応管にセットし,電気炉で加熱している触媒層の上部より反応ガスを供給,出口ガスとの成分差比較による活性試験,この一連の操作で行える触媒探索のフェーズはとっくに過ぎた。TWC(Three-Way Catalyst)にしてもNSR(NOx Storage Reduction)にしても,現実起こっていることは非定常反応であって,その制御の中で解を見つけている。ここに着目して,システム全体で触媒というものを見つめていかなければ,“環境触媒”実現の困難さに打ち勝てるシステムを提案し続けてはいけないのではないかと強く感じる。
自動車触媒をはじめ,“環境触媒”には,さまざまな方面からの要請がある。内燃機関によるエネルギー取得を基本としている我が国では,燃焼効率の増加に伴いシステムから排出される排ガスが低温化し,排ガス浄化のためにかけるエネルギーが増加することは必至である。さらには,排ガスの運転条件変動だけでなく,世界的なエネルギー・資源マップの時々刻々の変化によって使用燃料にも多種多様性,成分などの変化変動がある時代となる。それを御園生先生のオリジナル図に対して加筆したものが図1である。こういった状況にも関わらず,世界で一番厳しい環境規制が我が国には施行され,「何でも来い」的な入口にも関わらず,出口のハードルが極めて高い。しかも我が国は国土が狭く,何事もコンパクト化が望まれる。使い古された表現ではあるが,環境問題は環境-資源-エネルギーの三位一体で語られるべきであり,考える必要がある。こういった環境触媒への変動的要請に対して,やはり粛々と,活性—選択性—寿命という触媒三大要素を同時実現する触媒およびシステムとしての触媒技術に関する研究開発を続けていかねばならない。こういった諸問題に対して,ゼオライトはどのように関わっていけるか,積極的に見いだして行きたい。
本稿の最後を利用させていただき,これまでの共同研究者に謝意を申し上げたい。本研究のHCトラップの研究は,東京大学での恩師である教授大久保達也先生の研究室に助手(当時)として在籍している時,三菱自動車の棚田浩氏,安東弘光氏と共同研究をさせていただいた検討結果である。NO直接分解の検討に至る過程では,NO吸着に使用するOSDAフリーベータをご提供いただいた大久保先生ならびに板橋慶治氏のおかげで,このゼオライトがなければ達成できなかった触媒特性に辿り着けそうになっている。またベータゼオライト骨格内Al分布,金属イオンサイト分布の検討では,チェコサイエンスアカデミーのJiri Dedecek氏にお骨折りいただいた。MWの使用については,産業技術総合研究所東北センターの西岡将輝氏に全面的に指導していただいている。まずはこの方々に紙面をお借りして御礼申し上げたい。また,ここでは挙げられないくらいの数の東京大学小倉研究室スタッフならびに学生諸君にも,同程度以上の感謝を申し上げたい。そして,こういった研究が現在もなお行えているのも,筆者の早稲田大学時代の恩師である教授(現在名誉教授)菊地英一先生からのご指導が,今になっても活かされている気がして止まない。記して感謝したい。
また本研究の一部は,文部科学省から受託した元素戦略拠点形成型プロジェクト「触媒・電池の元素戦略研究拠点(ESICB)」に関するものである。